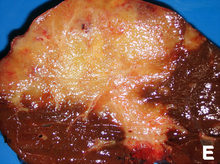
มะเร็งท่อน้ำดี
| มะเร็งท่อน้ำดี (Cholangiocarcinoma) | |
|---|---|
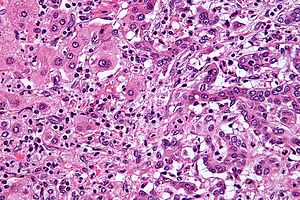 | |
| ภาพกล้องจุลทรรศน์ของมะเร็งท่อน้ำดีชนิดในตับ (ซีกขวาของภาพ) เทียบกับเซลล์ตับปกติ (ซีกซ้าย) สีย้อมเอชแอนด์อี | |
| การออกเสียง |
|
| สาขาวิชา | วิทยามะเร็ง |
| อาการ | ปวดท้อง, ดีซ่าน, น้ำหนักลด, คันทั่วร่าง, ไข้ |
| การตั้งต้น | 70 ปี |
| ประเภท | ในตับ, บริเวณขั้วตับ, ส่วนปลาย |
| ปัจจัยเสี่ยง | ท่อน้ำดีอักเสบแข็งปฐมภูมิ, ลำไส้ใหญ่อักเสบเป็นแผล, การติดเชื้อพยาธิใบไม้ตับบางชนิด การผิดรูปของตับแต่กำเนิดบางชนิด |
| วิธีวินิจฉัย | ยืนยันจากการตรวจเนื้องอกภายใต้กล้องจุลทรรศน์ |
| การรักษา | การผ่าตัดออก, เคมีบำบัด, รังสีบำบัด, การใส่ท่อค้ำยัน, การปลูกถ่ายตับ |
| พยากรณ์โรค | โดยทั่วไปเลว |
| ความชุก | 1–2 คนต่อ 100,000 คนต่อปี (โลกตะวันตก) 84.6 ต่อ 100000 ประชากร (ชาย) และ 36.8 ต่อ 100000 ประชากร (หญิง) (ประเทศไทย) |
มะเร็งท่อน้ำดี หรือ โคแลงจิโอคาร์ซิโนมา (อังกฤษ: cholangiocarcinoma) เป็นมะเร็งชนิดหนึ่งที่เกิดกับท่อน้ำดี อาการของโรค เช่น ปวดท้อง ดีซ่าน น้ำหนักลด คันทั่วร่าง และไข้ นอกจากนี้ อาจพบว่าอุจจาระสีจางและปัสสาวะสีเข้ม มะเร็งในตำแหน่งอื่น ๆ ที่นับเป็นมะเร็งท่อน้ำดี ได้แก่ มะเร็งถุงน้ำดี และมะเร็งของกระเปาะของวาเตอร์
ปัจจัยเสี่ยงของมะเร็งท่อน้ำดี เช่น ท่อน้ำดีอักเสบแข็งปฐมภูมิ ลำไส้ใหญ่อักเสบเป็นแผล ตับแข็ง ตับอักเสบซี ตับอักเสบบี การติดเชื้อพยาธิใบไม้ตับบางชนิด และการผิดรูปของตับบางชนิด อย่างไรก็ดี บุคคลส่วนใหญ่ไม่สามารถหาปัจจัยเสี่ยงได้ การวินิจฉัยเป็นการตั้งข้อสงสัยโดยอาศัยการทดสอบเลือด การถ่ายภาพทางการแพทย์ การส่องกล้องลำไส้ และบางทีรวมถึงการสำรวจโดยผ่าตัด ยืนยันโรคโดยการตรวจสอบเซลล์จากเนื้องอกภายใต้กล้องจุลทรรศน์ ตรงแบบเป็นมะเร็งชนิดต่อม
หากผู้ป่วยมะเร็งท่อน้ำดีมีอาการครบตามแบบฉบับ มักอยู่ในระยะที่ไม่สามารถรักษาให้หายขาดได้แล้ว ในผู้ป่วยเหล่านี้การรักษาประทังอาจได้แก่การผ่าตัดออก เคมีบำบัด รังสีบำบัด และการใส่ท่อค้ำยัน การผ่าตัดสามารถตัดเนื้องอกออกได้ในผู้ป่วยประมาณหนึ่งในสามที่มะเร็งเกิดที่ท่อน้ำดีรวม และน้อยกว่านั้นหากเกิดในตำแหน่งอื่น ทำให้มีโอกาสหายขาดได้ กระนั้นแม้ผ่าตัดออกได้สำเร็จ แต่โดยทั่วไปยังแนะนำเคมีบำบัดและรังสีบำบัดอยู่ ในผู้ป่วยบางส่วนอาจรักษาด้วยการผ่าตัดอาจปลูกถ่ายตับ แม้การผ่าตัดสำเร็จ แต่โดยทั่วไปแล้วจะมีโอกาสรอดชีวิต 5 ปีไม่ถึง 50%
มะเร็งท่อน้ำดีพบน้อยในโลกตะวันตก โดยมีอุบัติการณ์ต่อปีประมาณ 0.5–2 ต่อ 100,000 คนในโลกตะวันตก แต่อุบัติการณ์ของมะเร็งท่อน้ำดีในไทยกลับมีสูงมากที่สุดในโลก ในบางพื้นที่สูงถึง 60 ต่อ 100,000 คนต่อปี ตรงแบบเกิดในบุคคลวัย 70–79 ปี ทว่า ในผู้ป่วยท่อน้ำดีอักเสบแข็งปฐมภูมิ มะเร็งมักเกิดในบุคคลอายุ 40–49 ปี และในช่วงหลายสิบปีมานี้อัตราอุบัติการณ์ของมะเร็งท่อนำดีทั่วโลกกำลังเพิ่มขึ้น
อาการและอาการแสดง

สิ่งตรวจพบที่พบบ่อยที่สุดของมะเร็งท่อน้ำดีคือการมีผลการตรวจการทำงานของตับผิดปกติ ดีซ่าน (เกิดขึ้นเมื่อท่อน้ำดีถูกอุดตันโดยเนื้องอก) ปวดท้อง (30–50%) คันตามตัว (66%) น้ำหนักลด (30–50%) ไข้ (สูงสุด 20%) หรือสีอุจจาระหรือปัสสาวะเปลี่ยน อาการส่วนหนึ่งขึ้นอยู่กับตำแหน่งของเนื้องอก ผู้ป่วยมะเร็งท่อน้ำดีในท่อน้ำดีนอกตับมีโอกาสเกิดดีซ่านมากกว่า และผู้ป่วยที่เนื้องอกอยู่ในท่อน้ำดีในตับมักมีอาการปวดโดยไม่มีดีซ่านมากกว่า ในประเทศไทย พบว่าผู้ป่วยบางส่วนมาพบแพทย์ด้วยปัญหาก้อนในตับ (14%) คลำถุงน้ำดีได้ (6.7%) ถุงน้ำดีอักเสบเฉียบพลันแบบไม่มีนิ่วในถุงน้ำดี (7%) มีไข้ไม่ทราบสาเหตุ และพบโดยบังเอิญในขณะที่ผ่าตัดช่องท้องด้วยสาเหตุอื่น อาการค่อนข้างจะขึ้นอยู่กับตำแหน่งของเนื้องอก โดยผู้ป่วยที่มีเนื้องอกอยู่นอกตับมักจะมีอาการดีซ่าน ส่วนผู้ป่วยที่มีเนื้องอกอยู่ในตับมักมีอาการปวดโดยไม่มีดีซ่าน
ผลการตรวจการทำงานของตับในผู้ป่วยมะเร็งท่อน้ำดีมักพบว่ามีลักษณะของการอุดตันท่อน้ำดีโดยมีระดับบิลิรูบินหรือเอนไซม์ตับอย่างอัลคาไลน์ฟอสฟาเทสและแกมมา-กลูตามิลทรานสเฟอเรสสูงขึ้น โดยมีระดับเอนไซม์ตับทรานซามิเนส (Transaminase) ค่อนข้างปกติเมื่อเทียบกัน ผลการตรวจทางห้องปฏิบัติการเหล่านี้เป็นการแสดงว่าการอุดตันของน้ำท่อน้ำดีจะเป็นสาเหตุของดีซ่านมากกว่าจะเป็นจากการอักเสบหรือการติดเชื้อของตับ
ปัจจัยเสี่ยง
แม้ผู้ป่วยส่วนใหญ่จะไม่มีปัจจัยเสี่ยงชัดเจนแต่ก็ได้มีการศึกษาพบว่ามีปัจจัยเสี่ยงบางอย่างที่สัมพันธ์กับมะเร็งท่อน้ำดี ในโลกตะวันตกปัจจัยเสี่ยงที่พบมากที่สุดคือการเป็นโรคท่อน้ำดีอักเสบแข็งปฐมภูมิ (primary sclerosing cholangitis) ซึ่งเป็นโรคท่อน้ำดีอักเสบชนิดหนึ่งที่ทำให้มีการหนาแข็งของท่อน้ำดี โรคนี้มีความสัมพันธ์กับโรคลำไส้ใหญ่อักเสบแบบมีแผล (ulcerative colitis) อีกทีหนึ่ง การศึกษาวิจัยทางระบาดวิทยาแสดงให้เห็นว่าอัตราเสี่ยงตลอดชีวิตของผู้ป่วย PSC ที่จะเป็นมะเร็งท่อน้ำดีอยู่ที่ 10–15% ในขณะที่งานวิจัยชุดที่ได้จากการชันสูตรศพพบว่ามีอัตราสูงถึง 30% ส่วนกลไกที่ทำให้ผู้ป่วย PSC เป็นมะเร็งท่อน้ำดีมากขึ้นนั้นยังไม่ได้รับการอธิบายแน่ชัด
โรคติดเชื้อปรสิตบางชนิดก็เป็นปัจจัยเสี่ยงเช่นกัน เช่นการติดเชื้อพยาธิใบไม้ในตับ Opisthorchis viverrini (พบในประเทศไทย ลาว และมาเลเซีย) หรือ Clonorchis sinensis (พบในญี่ปุ่น เกาหลี และเวียดนาม) ซึ่งพบว่ามีความสัมพันธ์กับการเกิดมะเร็งท่อน้ำดี ผู้ป่วยโรคตับเรื้อรัง (chronic liver disease) ไม่ว่าจะจากการเป็นโรคตับอักเสบจากไวรัส (เช่น ไวรัสตับอักเสบบีหรือซี) โรคตับจากแอลกอฮอล์ หรือตับแข็งจากสาเหตุอื่น ต่างเพิ่มความเสี่ยงต่อการเป็นมะเร็งท่อน้ำดี งานวิจัยหนึ่งพบว่าการติดเชื้อเอชไอวีก็อาจเป็นปัจจัยเสี่ยงต่อการเป็นมะเร็งท่อน้ำดีเช่นกัน แม้ว่าจะยังไม่ชัดเจนว่าเป็นจากการติดเชื้อเอชไอวีเองหรือปัจจัยอื่นที่เกี่ยวข้อง (เช่น การติดเชื้อไวรัสตับอักเสบซี) ก็ตาม การติดเชื้อด้วยแบคทีเรียชนิด Helicobacter bilis และ Helicobacter hepaticus อาจเป็นสาเหตุของมะเร็งท่อน้ำดีได้
ความผิดปกติแต่กำเนิดของตับอย่างเช่นโรคแครอไล (Caroli disease) หรือถุงน้ำของท่อร่วมน้ำดี (choledochal cyst) มีความสัมพันธ์กับการเพิ่มความเสี่ยงตลอดชีวิตของการเป็นมะเร็งท่อน้ำดีประมาณ 15% โรคพันธุกรรมที่พบน้อยอย่างกลุ่มอาการลินช์ชนิดที่ 2 (Lynch syndrome II) และโรคติ่งเนื้อในท่อน้ำดี (biliary papillomatosis) ก็มีความสัมพันธ์กับมะเร็งท่อน้ำดี ส่วนการมีนิ่วในถุงน้ำดีนั้นยังไม่ชัดเจนว่าเป็นความเสี่ยงต่อการเกิดมะเร็งท่อน้ำดีหรือไม่ อย่างไรก็ดี โรคนิ่วในตับซึ่งพบน้อยในตะวันตกแต่พบได้บ่อยกว่าในบางส่วนของเอเชียกลับมีความสัมพันธ์กับมะเร็งท่อน้ำดีอย่างมาก รวมทั้งการรับประทานอาหารหมักดอง เช่น ปลาร้า ปลาเจ่า ปลาจ่อม รวมทั้งปลาส้ม จะมีสาร N-Nitrosocompound และไนโตรซามีน (nitrosamine) ซึ่งเป็นปัจจัยเสี่ยงให้เกิดมะเร็งท่อน้ำดีได้ การสัมผัสสารทึบรังสีบางชนิดเช่น ทอโรทราสต์ ซึ่งเป็นทอเรียมไดออกไซด์รูปแบบหนึ่งนั้นก็มีความสัมพันธ์กับการเป็นมะเร็งท่อน้ำดีที่เวลา 30–40 ปีหลังสัมผัส จึงสหรัฐห้ามใช้ไปแล้วตั้งแต่คริสต์ทศวรรษ 1950
พยาธิสรีรวิทยา
มะเร็งท่อน้ำดีอาจเกิดกับท่อน้ำดีตรงส่วนใดก็ได้ ทั้งในและนอกตับ เนื้องอกที่เกิดในท่อน้ำดีในตับจะถูกเรียกเป็นชนิด "ในตับ" (intrahepatic) ส่วนที่เกิดกับท่อน้ำดีนอกตับเรียก "นอกตับ" (extrahepatic) และเนื้องอกที่เกิดกับตำแหน่งที่ท่อน้ำดีออกจากตับพอดีเรียก บริเวณขั้วตับ (perihilar) มะเร็งท่อน้ำดีที่เกิดขึ้นที่ตำแหน่งที่ท่อตับข้างซ้ายและข้างขวามารวมกันเป็นท่อน้ำดีร่วมนั้นอาจเรียกว่าเนื้องอกคลาตสกิน (Klatskin tumor)
แม้จะเป็นที่ทราบกันดีว่ามะเร็งท่อน้ำดีเป็นอะดีโนคาร์ซิโนมาของเซลล์เยื่อบุผิวทางเดินน้ำดี แต่ก็ยังไม่เป็นที่ทราบชัดเจนว่าเซลล์ต้นกำเนิดคือเซลล์ใด แม้หลักฐานใหม่ ๆ ชี้ว่าอาจมีเซลล์ต้นกำเนิดเป็นสเต็มเซลล์หลายสรรพคุณในตับ (pluripotent hepatic stem cell) ก็ตาม เชื่อกันว่ามะเร็งท่อน้ำดีเกิดขึ้นได้จากการเกิดมะเร็งหลายระยะ ตั้งแต่มีการเจริญเกิน (hyperplasia) ในช่วงแรก กลายเป็นเมตาเพลเชีย (metaplasia) และเป็นการเจริญผิดปรกติ (dysplasia) และเกิดเป็นมะเร็งขึ้นในที่สุด ซึ่งเป็นกระบวนการที่ใกล้เคียงกับที่เกิดในการเกิดมะเร็งลำไส้ใหญ่ และเชื่อว่าการอักเสบเรื้อรังของท่อน้ำดี การอุดตันท่อน้ำดี และการมีน้ำดีคั่ง อาจมีส่วนในการเปลี่ยนแปลงเหล่านี้
ทางมิญชวิทยาพบว่าเซลล์มะเร็งท่อน้ำดีมีความแตกต่างทางการเปลี่ยนสภาพของเซลล์ (cell differentiation) ตั้งแต่ดี (well) ไปจนถึงแย่ (undifferentiated) ส่วนใหญ่ถูกล้อมรอบด้วยการตอบสนองแบบมีเนื้อเยื่อพังผืด (fibrotic tissue) และเนื้อเยื่อเดสโมพลาสติก (desmoplastic tissue) หากมีเนื้อเยื่อพังผืดมากอาจทำให้แยกเซลล์มะเร็งท่อน้ำดีที่มีการเปลี่ยนสภาพของเซลล์ดีออกจากเซลล์เนื้อเยื่อบุผิวที่ถูกกระตุ้น (reactive epithelium) ไม่ได้ ยังไม่มีสารย้อมทางอิมมูโนฮิสโตเคมี (immunohistochemistry) ตัวใดที่สามารถแยกเนื้อเยื่อท่อน้ำดีที่เป็นเนื้อร้ายออกจากเนื้อไม่ร้ายได้ แม้จะมีการย้อมสารไซโตเคราติน (cytokeratin) คาร์ซิโนเอมบริโอนิกแอนติเจน และมิวซินที่อาจช่วยในการวินิจฉัยได้บ้างก็ตาม เนื้องอกส่วนใหญ่ (>90%) เป็นมะเร็งชนิดต่อม
การวินิจฉัย
การตรวจเลือด
ยังไม่มีการตรวจเลือดที่จำเพาะต่อการวินิจฉัยมะเร็งท่อน้ำดี แม้ระดับของคาร์ซิโนเอมบริโอนิกแอนติเจนและซีเอ 19-9 อาจเพิ่มสูงได้แต่ก็ไม่ได้มีความไวหรือความจำเพาะมากพอที่จะใช้เป็นการตรวจคัดกรองได้ อย่างไรก็ดีการตรวจเหล่านี้อาจเป็นประโยชน์เมื่อใช้ร่วมกับการตรวจภาพรังสีเพื่อสนับสนุนว่ารอยโรคที่เห็นนั้นเป็นมะเร็งท่อน้ำดีหรือไม่
การตรวจภาพรังสีช่องท้อง

มักใช้การตรวจอัลตราซาวนด์ของตับและแขนงทางเดินน้ำดีมักถูกใช้เป็นตัวเลือกแรก ๆ ในการตรวจภาพรังสีสำหรับผู้ป่วยที่สงสัยว่ามีการอุดตันของทางเดินน้ำดี โดยสามารถตรวจพบการอุดตันและการขยายของท่อน้ำดีได้ บางครั้งก็สามารถได้ข้อมูลที่เพียงพอจะวินิจฉัยมะเร็งท่อน้ำดีได้ด้วยซีทีสแกนก็อาจมีส่วนสำคัญในการช่วยวินิจฉัยมะเร็งท่อน้ำดีด้วยได้
การตรวจภาพของแขนงทางเดินน้ำดี
แม้การถ่ายภาพรังสีของช่องท้องจะมีประโยชน์ในการช่วยการวินิจฉัยมะเร็งท่อน้ำดี แต่บ่อยครั้งการดูภาพของท่อน้ำดีโดยตรงก็มีความจำเป็น การถ่ายภาพรังสีท่อน้ำดีและตับอ่อนย้อนทางแบบส่องกล้อง (ERCP) ซึ่งเป็นการตรวจโดยการใช้กล้องส่องทางเดินอาหารทำโดยแพทย์ผู้เชี่ยวชาญระบบทางเดินอาหารหรือศัลยแพทย์ที่ได้รับการฝึกฝนพิเศษ เป็นการตรวจที่ใช้กันทั่วไปเพื่อจุดประสงค์นี้ แม้ ERCP จะเป็นการตรวจที่ค่อนข้างรุกล้ำผู้ป่วยและมีความเสี่ยงอยู่ในระดับหนึ่ง แต่ผลดีที่มีคือทำให้สามารถตัดชิ้นเนื้อส่งตรวจทางพยาธิวิทยาได้ สามารถวางท่อคงรูป (stent) ไว้เพื่อใช้ในวิธีการอื่น ๆ เพื่อลดการอุดตันทางเดินน้ำดีได้ นอกจากนี้ยังสามารถทำการตรวจอัลตราซาวนด์ผ่านการส่องกล้อง (endoscopic ultrasound) ไปพร้อมกันด้วยได้เพื่อเพิ่มความแม่นยำของการตัดชิ้นเนื้อส่งตรวจทางพยาธิวิทยาและให้ข้อมูลเกี่ยวกับการแพร่กระจายมายังต่อมน้ำเหลืองและการประเมินว่าจะสามารถรักษาด้วยการผ่าตัดได้หรือไม่ด้วย นอกจากการใช้ ERCP แล้วยังมีการใช้การสร้างภาพท่อน้ำดีด้วยการเจาะผ่านผิวหนังและตับ (percutaneous transhepatic cholangiography, PTC) ได้ การสร้างภาพทางเดินน้ำดีและตับอ่อนด้วยเรโซแนนซ์แม่เหล็ก (magnetic resonance cholangiopancreatography, MRCP) ก็เป็นอีกวิธีหนึ่งที่ไม่ทำให้การรุกล้ำผู้ป่วยซึ่งใช้แทน ERCP ได้ ผู้เชี่ยวชาญบางท่านเสนอว่าควรใช้ MRCP แทน ERCP ในการวินิจฉัยมะเร็งท่อน้ำดี เนื่องจากสามารถแสดงให้เห็นขอบเขตของเนื้องอกได้แม่นยำกว่าและลดความเสี่ยงที่เกิดจากการใช้ ERCP ด้วย
การผ่าตัด
บางครั้งอาจจำเป็นต้องมีการผ่าตัดสำรวจช่องท้อง (surgical exploration) เพื่อให้สามารถได้ชิ้นเนื้อที่เหมาะสมกับการส่งตรวจทางพยาธิวิทยาและเพื่อให้สามารถประเมินระยะของผู้ป่วยมะเร็งท่อน้ำดีได้เหมาะสม การผ่าตัดด้วยการส่องกล้อง (laparoscopy) สามารถใช้เพื่อการประเมินระยะได้ และอาจสามารถลดความจำเป็นของการผ่าตัดที่รุกล้ำผู้ป่วยมากกว่าอย่างการผ่าตัดเปิดช่องท้อง (laparotomy) ได้ในผู้ป่วยบางราย นอกจากนี้การผ่าตัดยังเป็นวิธีการรักษาให้หายเพียงทางเดียวของมะเร็งท่อน้ำดี แต่ก็ทำได้กับเฉพาะโรคระยะแรกเริ่มเท่านั้น
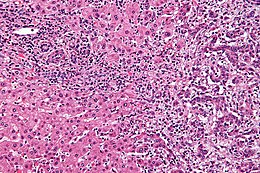
พยาธิวิทยา
ทางมิญชวิทยาพบว่ามะเร็งท่อน้ำดีมักแบ่งเป็นชนิดที่มีการเปลี่ยนสภาพของเซลล์ดี (well) และปานกลาง (moderate) การตรวจทาง immunohistochemistry มีประโยชน์ในการช่วยวินิจฉัย และช่วยในการแยกว่าเนื้องอกนั้นกำเนิดจากท่อน้ำดีหรือแพร่กระจายมาจากอวัยวะอื่นในระบบทางเดินอาหาร การขูดเซลล์ตรวจ (cytological scraping) มักไม่ช่วยในการวินิจฉัย
การแบ่งระยะ
แม้จะมีระบบการแบ่งระยะของมะเร็งท่อน้ำดีอยู่ไม่ต่ำกว่า 3 แบบ ก็ตาม (Bismuth, Blumgart, American Joint Committee on Cancer) แต่ไม่มีระบบใดที่แสดงให้เห็นว่ามีประโยชน์ช่วยทำนายอัตราการรอดชีวิตได้ ส่วนที่สำคัญที่สุดของการกำหนดระยะคือเพื่อให้ทราบว่าเนื้องอกนั้นยังสามารถผ่าตัดเอาออกได้หรือลุกลามไปมากจนไม่สามารถผ่าตัดได้ บ่อยครั้งที่การประเมินนี้จะทำได้ก็จนกว่าลงมือผ่าตัดแล้วเท่านั้น
แนวทางทั่วไปในการประเมินว่าสามารถผ่าตัดออกได้หรือไม่ ได้แก่
- การไม่มีการแพร่กระจายของมะเร็งไปยังต่อมน้ำเหลืองหรือตับ
- การไม่มีการลุกลามของมะเร็งไปยังหลอดเลือดดำพอร์ทัลของตับ
- การไม่มีการลุกลามของมะเร็งไปยังอวัยวะข้างเคียงโดยตรง
- การไม่มีการแพร่กระจายของมะเร็งไปยังอวัยวะที่อยู่ไกล
การรักษา
หากไม่สามารถผ่าตัดเอาเนื้องอกออกได้ทั้งหมด มะเร็งท่อน้ำดีก็ถือเป็นมะเร็งที่ไม่มีทางรักษาให้หายได้ ด้วยเหตุว่าการประเมินว่าผ่าตัดเนื้องอกได้หรือไม่ในผู้ป่วยส่วนใหญ่นั้นต้องสำรวจระหว่างผ่าตัดวิธีเดียวเท่านั้น ทำให้ผู้ป่วยจำนวนมากต้องได้รับการผ่าตัดสำรวจช่องท้อง เว้นเสียแต่มีข้อบ่งชี้ชัดเจนแล้วว่าเนื้องอกนั้นอยู่ในระยะที่ไม่สามารถรักษาได้โดยการผ่าตัด อย่างไรก็ดี มาโยคลินิกรายงานความสำเร็จอย่างมีนัยสำคัญในการรักษามะเร็งท่อน้ำดีระยะเริ่มต้นด้วยการปลูกถ่ายตับโดยใช้แนวทางเข้าสู่แบบ protocolized และมีเกณฑ์คัดเลือกที่เข้มงวด
การบำบัดตัวเสริมหลังการปลูกถ่ายตับอาจมีที่ใช้ในการรักษาผู้ป่วยที่ผ่าตัดไม่ได้บางคน การบำบัดที่จำกัดอยู่เฉพาะบางบริเวณ (locoregional) นั้น ได้แก่ การให้สิ่งอุดหลอดเลือดเคมีทางหลอดเลือดแดง (transarterial chemoembolization, TACE) การให้สิ่งอุดหลอดเลือดรังสีทางหลอดเลือดแดง (transarterial radioembolization, TARE) และการบำบัดลอกอาจมีที่ใช้ในมะเร็งท่อน้ำดีชนิดในตับเพื่อให้การรักษาประทังหรืออาจมีโอกาสหายในผู้ป่วยที่ไม่ควรรับการผ่าตัด
การรักษาร่วมด้วยเคมีบำบัดและรังสีรักษา
ถ้าสามารถผ่าตัดเอาเนื้องอกออกได้ ผู้ป่วยอาจต้องได้รับการรักษาด้วยเคมีบำบัดร่วม (adjuvant chemotherapy) หรือรังสีรักษาร่วม (adjuvant radiation therapy) หลังการผ่าตัดเพื่อเพิ่มโอกาสการรักษาหายขาด หากขอบชิ้นเนื้อไม่มีเซลล์มะเร็ง (negative tissue margins) หรือสามารถตัดชิ้นมะเร็งออกได้ทั้งหมดแล้วการรักษาร่วมเหล่านี้อาจให้ประโยชน์หรือไม่นั้นยังไม่ได้ข้อสรุป มีการศึกษาวิจัยที่ให้ผลทั้งว่าการรักษาร่วมในกรณีเช่นนี้มีประโยชน์และไม่มีประโยชน์ และจนถึงเดือนมีนาคม ค.ศ. 2007 ก็ยังไม่มีการศึกษาวิจัยแบบการวิจัยเชิงทดลองแบบสุ่มและมีกลุ่มควบคุมของเรื่องนี้ออกมา ส่วนบทบาทของการใช้การรักษาทั้งเคมีบำบัดและรังสีรักษาร่วม (combined chemoradiotherapy) ในสถานการณ์เช่นนี้นั้นยังไม่เป็นที่แน่ชัด อย่างไรก็ดี หากผลขอบชิ้นเนื้อพบมีเซลล์มะเร็ง (positive margin) จะเป็นการบ่งชี้ว่ายังไม่สามารถเอาก้อนเนื้องอกออกได้หมดด้วยการผ่าตัด ดังนั้นการรักษาร่วมด้วยการฉายรังสี (และอาจรวมถึงเคมีบำบัด) ในกรณีเช่นนี้จึงได้รับการยอมรับโดยทั่วไปตามข้อมูลที่มีอยู่ในปัจจุบัน
การรักษาโรคในระยะลุกลาม
ผู้ป่วยมะเร็งท่อน้ำดีจำนวนมากได้รับการวินิจฉัยโรคเมื่อโรคลุกลามไปมากถึงระยะที่ไม่สามารถรักษาได้ด้วยการผ่าตัดแล้วซึ่งผู้ป่วยเหล่านี้มักได้รับการรักษาด้วยเคมีบำบัดแบบบรรเทาอาการ (palliative chemotherapy) โดยอาจใช้ร่วมกับรังสีรักษา มีการวิจัยเชิงทดลองแบบสุ่มและมีกลุ่มควบคุมที่รับรองการรักษาด้วยเคมีบำบัดแล้วว่าสามารถเพิ่มคุณภาพชีวิตและยืดอายุขัยของผู้ป่วยมะเร็งท่อน้ำดีระยะที่ไม่สามารถรักษาด้วยการผ่าตัดได้ แต่ยังไม่มีสูตรการรักษาใด ๆ ที่ได้รับการยอมรับเป็นมาตรฐานสากล ทำให้ปัจจุบันยังมีคำแนะนำให้มีการทดลองหาวิธีใหม่ ๆ ในการรักษาต่อไปอีก ยาเคมีบำบัดที่ใช้รักษามะเร็งท่อน้ำดีมีเช่น 5-fluorouracil ร่วมกับ leucovoringemcitabine ตัวเดียว หรือ gemcitabine ร่วมกับ cisplatinirinotecan หรือ capecitabine การศึกษาวิจัยนำร่องบางชิ้นชี้ว่าผู้ป่วยมะเร็งท่อน้ำดีระยะลุกลามอาจได้รับประโยชน์จากยากลุ่มสารยับยั้งไทโรซีนไคเนส (tyrosine kinase inhibitors) อย่าง erlotinib
การรักษาด้วย Photodynamic therapy เป็นการรักษาเชิงทดลองอย่างหนึ่งซึ่งฉีดสารไวแสง (light-sensitizing agent) เข้าไปในร่างกายผู้ป่วย จากนั้นจึงส่งคลื่นแสงเข้าไปยังเนื้องอกโดยตรงผ่านกล้องส่อง การรักษาวิธีนี้มีผลแสดงในการวิจัยเชิงทดลองแบบสุ่มและมีกลุ่มควบคุมขนาดเล็กสองชิ้นว่าได้ผล แต่ยังไม่เป็นที่แน่ชัดว่าการรักษาด้วยวิธีนี้จะมีบทบาทอย่างไรในการดูแลผู้ป่วยมะเร็งท่อน้ำดี
พยากรณ์โรค
การรักษาด้วยการผ่าตัดเอาก้อนเนื้อออกยังคงเป็นวิธีการรักษาเพียงวิธีเดียวของมะเร็งท่อน้ำดีที่มีโอกาสหาย สำหรับผู้ป่วยที่ไม่สามารถรักษาได้ด้วยการผ่าตัดเนื่องจากตรวจพบว่ามีการแพร่กระจายไปยังต่อมน้ำเหลืองบริเวณไกลนั้นอัตรารอดชีวิตที่ 5 ปี (5-year survival rate) อยู่ที่ 0%, และโดยทั่วไปอยู่ที่ 5% ค่ามัธยฐานการรอดชีวิตโดยภาพรวม (overall median duration of survival) สำหรับผู้ป่วยที่ไม่สามารถรักษาได้ด้วยการผ่าตัด ไม่ได้รับการรักษา สุขภาพอื่นปกติ และมีเนื้องอกอยู่ในตับผ่านทางท่อน้ำดีในตับและหลอดเลือดดำพอร์ทัลตับ (hepatic portal vein) อยู่ที่น้อยกว่า 6 เดือน
สำหรับผู้ป่วยที่สามารถรักษาได้ด้วยการผ่าตัด โอกาสของการรักษาหายขาดได้นั้นแตกต่างกันไปขึ้นอยู่กับตำแหน่งของเนื้องอกและอยู่ที่ว่าสามารถผ่าเอาเนื้องอกนั้นออกได้ทั้งหมดหรือบางส่วน มะเร็งท่อน้ำดีส่วนปลาย ซึ่งเจริญขึ้นจากท่อน้ำดีร่วมนั้นส่วนใหญ่สามารถรักษาได้ด้วยวิธีการผ่าตัดแบบวิปเปิล (Whipple procedure) โดยมีอัตราการรอดชีวิตระยะยาว (long-term survival rate) อยู่ที่ระหว่าง 15–25% รายงานชุดหนึ่งกล่าวว่าอัตราการรอดชีวิตที่ 5 ปีของผู้ป่วยที่ไม่มีการแพร่กระจายของโรคไปยังต่อมน้ำเหลืองนั้นอยู่ที่ 54% มะเร็งท่อน้ำดีในตับ ซึ่งเจริญขึ้นมาจากท่อน้ำดีส่วนที่อยู่ในเนื้อตับนั้นส่วนใหญ่รักษาด้วยการตัดเอาเนื้อตับออกบางส่วน มีรายงานหลายชุดกล่าวว่าโอกาสการรอดชีวิตหลังรับการรักษาด้วยการผ่าตัดอยู่ที่ 22-66% โดยผลการรักษาอาจแตกต่างกันไปขึ้นอยู่กับว่ามีการแพร่กระจายของมะเร็งไปยังต่อมน้ำเหลืองหรือไม่และการผ่าตัดนั้นสามารถเอาเนื้อมะเร็งออกได้หมดหรือไม่ มะเร็งท่อน้ำดีที่อยู่บริเวณขั้วตับ (perihilar cholangiocarcinoma) ซึ่งเจริญขึ้นมาจากบริเวณตำแหน่งที่ท่อน้ำดีออกมาจากตับนั้นมีโอกาสรักษาได้ด้วยการผ่าตัดน้อยกว่า ในกรณีที่สามารถผ่าตัดได้ส่วนใหญ่ก็ต้องผ่าตัดกินบริเวณกว้าง (aggressive) โดยมักต้องผ่าตัดเอาถุงน้ำดีออก และอาจต้องผ่าตัดเอาบางส่วนของตับออกด้วย ผู้ป่วยมะเร็งท่อน้ำดีบริเวณขั้วตับที่สามารถรักษาได้ด้วยการผ่าตัดนั้นมีรายงานอัตราการรอดชีวิตที่ 5 ปีอยู่ที่ระหว่าง 20–50%
พยากรณ์โรคอาจแย่ลงไปอีกสำหรับผู้ป่วยมะเร็งท่อน้ำดีที่เป็นโรคท่อน้ำดีอักเสบแข็งปฐมภูมิอยู่ก่อน ซึ่งน่าจะมีเหตุผลมาจากการที่กว่าจะรู้ว่าเป็นโรคก็เป็นระยะที่โรคลุกลามไปมากแล้ว หลักฐานบางชิ้นชี้ว่าผลการรักษาอาจดีกว่าหากได้รับการรักษาผ่าตัดแบบกินบริเวณกว้าง (aggressive) ร่วมกับการบำบัดตัวเสริม
วิทยาการระบาด
| ประเทศ | ในตับ (ชาย/หญิง) | นอกตับ (ชาย/หญิง) |
|---|---|---|
| สหรัฐ | 0.60/0.43 | 0.70/0.87 |
| ญี่ปุ่น | 0.23/0.10 | 5.87/5.20 |
| ออสเตรเลีย | 0.70/0.53 | 0.90/1.23 |
| อังกฤษ/เวลส์ | 0.83/0.63 | 0.43/0.60 |
| สกอตแลนด์ | 1.17/1.00 | 0.60/0.73 |
| ฝรั่งเศส | 0.27/0.20 | 1.20/1.37 |
| อิตาลี | 0.13/0.13 | 2.10/2.60 |
มะเร็งท่อน้ำดีเป็นมะเร็งชนิดที่พบค่อนข้างน้อย มีผู้ป่วยได้รับวินิจฉัยในสหรัฐ 2,000 ถึง 3,000 คนต่อปี หรือคิดเป็นอุบัติการณ์ต่อปี 1–2 ต่อ 100,000 คน ประเทศไทยเป็นประเทศที่มีอุบัติการณ์ของมะเร็งท่อน้ำดีสูงที่สุดในโลก คืออยู่ที่ 84.6 ต่อ 100,000 ประชากรชาย และ 36.8 ต่อ 100,000 ประชากรหญิงในภาคตะวันออกเฉียงเหนือของประเทศไทย ข้อมูลโรงพยาบาลศรีนครินทร์ จังหวัดขอนแก่นรายงานว่าพบมะเร็งท่อน้ำดีในตับเป็นอันดับ 1 ของมะเร็งที่กำเนิดขึ้นในตับ มีอุบัติการณ์ 300 รายต่อปี การผ่าศพเป็นชุดรายงานความชุกระหว่าง 0.01% ถึง 0.46% มีความชุกของมะเร็งท่อน้ำดีในทวีปเอเชียสูงกว่า ซึ่งระบุว่าสาเหตุมาจากการติดเชื้อพยาธิใบไม้ตับบางชนิด อุบัติการณ์ของมะเร็งท่อน้ำดีเพิ่มขึ้นตามอายุ และพบในชายบ่อยกว่าหญิงเล็กน้อย (อาจเนื่องจากมีอัตราเกิดท่อน้ำดีอักเสบแข็งปฐมภูมิในชายสูงกว่าหญิงซึ่งเป็นปัจจัยเสี่ยงสำคัญ) ความชุกของมะเร็งท่อน้ำดีในผู้ป่วยท่อน้ำดีอักเสบแข็งปฐมภูมิอาจสูงถึง 30% จากการศึกษาด้วยการผ่าศพ
งานวิจัยหลายชิ้นแสดงให้เห็นว่ากำลังมีการเพิ่มขึ้นของอุบัติการณ์ของมะเร็งท่อน้ำดีในตับในช่วงหลายทศวรรษที่ผ่านมา โดยพบผู้ป่วยเพิ่มขึ้นในทวีปอเมริกาเหนือ ยุโรป เอเชีย และออสเตรเลีย สาเหตุที่ทำให้มีการเพิ่มขึ้นของอุบัติการณ์นี้ยังไม่แน่ชัดโดยอาจเป็นจากการพัฒนาของกระบวนการการวินิจฉัยก็เป็นได้ แต่ในขณะเดียวกันความชุกของปัจจัยที่อาจเป็นปัจจัยเสี่ยงของมะเร็งท่อน้ำดีเช่นการติดเชื้อเอชไอวีนั้นก็มีการเพิ่มขึ้นในช่วงเวลาที่ว่านี้เช่นกัน
แหล่งข้อมูลอื่น
|
คอมมอนส์ มีภาพและสื่อเกี่ยวกับ: มะเร็งท่อน้ำดี |
- ศูนย์วิจัยพยาธิใบไม้ตับและมะเร็งท่อน้ำดี เก็บถาวร 2010-07-17 ที่ เวย์แบ็กแมชชีน ของ มหาวิทยาลัยขอนแก่น
- American Cancer Society Detailed Guide to Bile Duct Cancer เก็บถาวร 2007-03-10 ที่ เวย์แบ็กแมชชีน.
- ข้อมูลเกี่ยวกับมะเร็งท่อน้ำดีนอกตับสำหรับผู้ป่วย จาก National Cancer Institute.
- The Cholangiocarcinoma Foundation: แหล่งข้อมูลสำหรับผู้ป่วยมะเร็งท่อน้ำดี ญาติมิตร ผู้ดูแล
- The Alan Morement Memorial Fund มูลนิธิของโรคมะเร็งท่อน้ำดีในอังกฤษ
- Macmillan/Cancerbackup page on Cholangiocarcinoma
| ทางเดินอาหาร |
|
||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Accessory |
|
||||||||||||||||||
| เยื่อบุช่องท้อง | |||||||||||||||||||
| |||||||||||||||||||
| เยื่อบุผิว |
|
||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ต่อม |
|
||||||||||||||||||||||||||||||
| อื่น ๆ |
|
||||||||||||||||||||||||||||||