วัคซีนดีเอ็นเอ

วัคซีนดีเอ็นเอ (อังกฤษ: DNA vaccine) เป็นวัคซีนประเภทที่นำ (transfect) ลำดับดีเอ็นเอซึ่งเข้ารหัสแอนติเจนอย่างหนึ่งโดยเฉพาะเข้าไปในเซลล์ของสิ่งมีชีวิตเพื่อกระตุ้นให้ภูมิคุ้มกันตอบสนอง
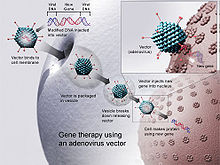
วัคซีนออกฤทธิ์โดยนำพลาสมิดเข้าไปในเซลล์ พลาสมิดได้สร้างขึ้นผ่านพันธุวิศวกรรมให้มีดีเอ็นเอซึ่งเข้ารหัสแอนติเจนที่ต้องการให้ภูมิคุ้มกันตอบสนอง โดยเซลล์จะเป็นผู้ผลิตแอนติเจนเอง วัคซีนนี้อาจมีข้อดีกว่าวัคซีนปกติ รวมทั้ง "ก่อการตอบสนองของภูมิคุ้มกันหลายรูปแบบอย่างครอบคลุมกว่า" มีวัคซีนดีเอ็นเอหลายอย่างที่ได้ทดสอบเพื่อใช้ในสัตว์แล้ว ซึ่งในบางกรณีก็ก่อภูมิคุ้มกันโรคได้จริง ๆ แต่ในบางกรณีก็ไม่ได้ มีงานวิจัยที่พยายามใช้เทคโนโลยีนี้เพื่อป้องกันโรคในมนุษย์ รวมทั้งโรคจากไวรัส แบคทีเรีย ปรสิต และมะเร็ง ในเดือนสิงหาคม 2021 รัฐบาลอินเดียได้อนุมัติให้ใช้วัคซีนโควิด-19 ชนิดดีเอ็นเอคือ ZyCoV-D ในภาวะฉุกเฉิน บริษัทยาอินเดียคือ Cadila Healthcare เป็นผู้พัฒนา เป็นวัคซีนดีเอ็นเอแรกในโลกที่อนุมัติให้ใช้กับมนุษย์
ข้อมูลพื้นฐาน
วัคซีนธรรมดาอาจมีส่วนประกอบเป็นแอนติเจนโดยเฉพาะ ๆ จากจุลชีพก่อโรค หรืออาจเป็นไวรัสก่อโรคที่ลดฤทธิ์ซึ่งกระตุ้นให้ภูมิคุ้มกันตอบสนอง วัคซีนดีเอ็นเอเป็นวัคซีนสารพันธุกรรม (genetic vaccine) เพราะมีข้อมูลทางพันธุกรรม (เป็นดีเอ็นเอหรืออาร์เอ็นเอ) ที่เข้ารหัสโปรตีนของจุลชีพที่มีภาวะเป็นแอนติเจน วัคซีนดีเอ็นเอมีดีเอ็นเอที่เข้ารหัสแอนติเจนโดยเฉพาะ ๆ จากจุลชีพก่อโรค เมื่อฉีดเข้าไปในร่างกายแล้วเข้าไปในเซลล์ กระบวนการธรรมชาติของเซลล์ก็จะสังเคราะห์โปรตีนอาศัยรหัสพันธุกรรมในพลาสมิดที่นำเข้าไปในเซลล์ เพราะโปรตีนเช่นนี้มีลำดับกรดอะมิโนที่เป็นลักษณะพิเศษของแบคทีเรียหรือไวรัส จึงทำให้ร่างกายรู้ได้ว่าเป็นสิ่งแปลกปลอม เมื่อเซลล์ผลิตโปรตีนเช่นนี้แล้วส่งไปที่ผิวเซลล์ ระบบภูมิคุ้มกันก็จะรู้ตัวแล้วเริ่มตอบสนอง
ประวัติ
ในปี 1983 นักไวรัสวิทยาที่กระทรวงสาธารณสุขรัฐนิวยอร์กได้ประดิษฐ์วิธีทางพันธุวิศวกรรมเพื่อสร้างวัคซีนดีเอ็นเอรวมใหม่ (recombinant DNA) คือได้แปลงวัคซีนฝีดาษธรรมดาให้เป็นวัคซีนที่สามารถใช้ป้องกันโรคอื่น ๆ ทำโดยแทรกยีนหนึ่งจากไวรัสอื่น ๆ (ได้แก่ไวรัสเริม ไวรัสตับอักเสบบี และไวรัสไข้หวัดใหญ่) ต่อมาในปี 1993 นักเคมีชีวภาพที่แหล็บวิจัยของบริษัทเมอร์คได้แสดงว่า การฉีดพลาสมิดที่เข้ารหัสยีนแอนติเจนของไข้หวัดใหญ่สามารถป้องกันหนูไม่ให้ติดโรค (ที่จงใจทำให้ติด) ต่อมาในปี 2016 สถาบันสุขภาพแห่งชาติสหรัฐได้เริ่มทดลองวัคซีนดีเอ็นเอเพื่อป้องกันไวรัสซิกาในมนุษย์ ซึ่งมีแผนรับอาสาสมัคร 120 คนอายุระหว่าง 18-35 ปี วัคซีนจะฉีดเข้าที่ต้นแขนด้วยความดันสูง แต่จนถึงเดือนสิงหาคม 2016 การผลิตวัคซีนให้ได้มาก ๆ ก็ยังไม่ลงตัว อนึ่ง บริษัท Inovio Pharmaceuticals และ GeneOne Life Science ได้เริ่มทดลองวัคซีนดีเอ็นเออีกชนิดสำหรับไวรัสซิกาในเมืองไมแอมี การทดลองวัคซีนดีเอ็นเอป้องกันโรคเอชไอวีก็กำลังดำเนินการอยู่อีกด้วย
ในเดือนสิงหาคม 2021 รัฐบาลอินเดียได้ลงทะเบียนให้ใช้วัคซีนดีเอ็นเอ ZyCoV-D ในภาวะฉุกเฉินเพื่อป้องกันโรคโควิด-19 โดยบริษัทยาอินเดีย Cadila Healthcare ได้พัฒนาวัคซีนนี้ขึ้น
การประยุกต์ใช้
จนถึงปี 2021 ยังไม่มีวัคซีนดีเอ็นเอที่อนุมัติให้ใช้กับมนุษย์ในสหรัฐ มีการทดลองน้อยมากที่กระตุ้นให้ภูมิคุ้มกันตอบสนองได้พอป้องกันโรค ดังนั้น เทคโนโลยีนี้จึงยังต้องพิสูจน์ว่ามีประสิทธิผลในมนุษย์หรือไม่ต่อไป แต่ก็มีวัคซีนดีเอ็นเอป้องกันโรคของม้าที่ได้อนุมัติแล้ว อนึ่ง กำลังมีการตรวจสอบด้วยว่าสามารถใช้เทคนิคนี้เพื่อแก้พิษงูได้หรือไม่ เทคโนโลยีนี้ยังสามารถใช้กระตุ้นให้ร่างกายสร้างแอนติบอดีเพื่อรักษาโรคในทำนองเดียวกับสารภูมิต้านทานโมโนโคลนอีกด้วย
ข้อดี
- ไม่เสี่ยงทำให้ติดโรค
- โมเลกุลทั้งแบบ MHC class I และ MHC class II จะเป็นตัวนำแอนติเจนไปแสดงที่ผิวเซลล์
- สามารถเลือกชักนำให้เซลล์ทีแบบ TH1 หรือ TH2 ตอบสนอง
- ภูมิคุ้มกันจะตอบสนองต่อแอนติเจนอย่างจำเพาะ
- พัฒนาและผลิตได้ง่ายกว่า
- เก็บและขนส่งได้โดยไม่เสื่อม
- มีราคาไม่แพง
- ไม่ต้องสังเคราะห์เพปไทด์ ไม่ต้องเพาะหรือทำโปรตีนรวมใหม่ (recombinant protein) ให้บริสุทธิ์ หรือเติมสารเสริมภูมิคุ้มกันที่เป็นพิษ
- สารอิมมูโนเจน/แอนติเจนที่ชักนำให้เกิดจะมีอยู่เป็นระยะเวลานาน
- ร่างกาย (in vivo) เป็นผู้ผลิตโปรตีนเอง จึงได้โปรตีนที่เหมือนธรรมชาติมากกว่า
ข้อเสีย
- จำกัดใช้กับสารอิมมูโนเจน (immunogen) หรือแอนติเจนที่เป็นโปรตีน ไม่สามารถใช้กับแอนติเจนที่ไม่ใช่โปรตีน เช่น พอลิแซ็กคาไรด์ของแบคทีเรีย
- ร่างกายอาจตอบสนองต่อโปรตีนของแบคทีเรียหรือของปรสิตอย่างไม่คาดหมาย
- ยาฉีดจมูกแบบอนุภาคนาโนซึ่งเป็นพลาสมิดประกอบด้วยดีเอ็นเออาจมีผลต่อเซลล์ชนิดอื่นซึ่งไม่ได้ตั้งใจ เช่นเซลล์สมอง
- วัคซีนต่าง ๆ ที่เพาะด้วยสิ่งมีชีวิตอาจปนเปื้อนกันเมื่อผลิตในโรงงานเดียวกัน
มีพาหะ (เวกเตอร์) เป็นพลาสมิด
การออกแบบ
วัคซีนดีเอ็นเอก่อการตอบสนองของภูมิคุ้มกันได้ดีสุดเมื่อใช้พาหะพันธุกรรมชนิดที่เซลล์แสดงออกเป็นโปรตีนได้จำนวนมากที่สุด ปกติจะเป็นพลาสมิดอันประกอบด้วยส่วน viral promoter ที่ดีซึ่งขับการถอดรหัสและการแปลรหัสยีน (หรือ complementary DNA) ที่ต้องการ โดยอาจรวมส่วน Intron A (Interferon alfa-2b) เข้าด้วยเพื่อเพิ่มเสถียรภาพของเอ็มอาร์เอ็นเอแล้วเพิ่มการแสดงออกของโปรตีน อนึ่ง ยังอาจรวมเอาส่วน termination signal หรือ polyadenylation ที่ขับการแสดงออกโปรตีนได้ดี เช่น ฮอร์โมนควบคุมการเจริญเติบโตของวัว (bovine growth hormone) หรือ beta globulin ของกระต่าย พาหะซึ่งมียีนหลายยีนที่ต้องการซึ่งเรียกว่า polycistronic vector บางครั้งจะทำขึ้นเพื่อให้แสดงออกอิมมูโนเจนมากกว่าหนึ่งอย่าง หรือให้แสดงออกอิมมูโนเจนบวกกับโปรตีนร่วมกระตุ้นภูมิคุ้มกัน (immunostimulatory protein)
เพราะพลาสมิดสามารถบรรจุรหัสพันธุกรรมได้เพียง ~200 Kbp การออกแบบให้สามารถแสดงออกโปรตีนได้ดีสุดจึงจำเป็น วิธีหนึ่งก็คือปรับใช้โคดอนภายในเอ็มอาร์เอ็นเอของจุลชีพก่อโรคให้ได้ดีสุดสำหรับเซลล์ยูแคริโอต คือ จุลชีพก่อโรคมักมี GC-content (guanine-cytosine content) ในอัตราที่ต่างกับสิ่งมีชีวิตที่เป็นเป้า ดังนั้น การเปลี่ยนลำดับยีนของอิมมูโนเจนให้มีโคดอนเหมือนกับที่มักเกิดในสิ่งมีชีวิตอาจทำให้แสดงออกโปรตีนได้ดีกว่า
ประเด็นที่ต้องพิจารณาอีกอย่างก็คือการเลือกลำดับ promoter นักวิทยาศาสตร์ได้ใช้ลำดับยีนที่เรียกว่า SV40 promoter ที่อาจก่อเนื้องอกในลิงและมนุษย์ จนกระทั่งพบว่าส่วน promoter จากไวรัสก่อมะเร็งไก่ คือ Rous Sarcoma Virus มีอัตราการแสดงออกที่สูงกว่า ต่อมาไม่นานนี้จึงพบว่า สามารถเพิ่มอัตราการแสดงออกและการตอบสนองทางภูมิคุ้มกันในสัตว์ตัวแบบโดยใช้ส่วน immediate-early (MIE) promoter ของซัยโตเมกาโลไวรัส (CMV) และใช้ cis-acting transcriptional element (หรือ cis-regulatory element) จากรีโทรไวรัส (retrovirus) วิธีเพิ่มอัตราการแสดงออกของโปรตีนอื่น ๆ รวมทั้งการการแทรกลำดับ enhancer sequence, อินทรอนสังเคราะห์ (synthetic introns), ลำดับ tripartite leader (TPL) จากอะดีโนไวรัส และการเปลี่ยนปรับปรุงส่วน polyadenylation และ termination signal ตัวอย่างพลาสมิดสำหรับวัคซีนดีเอ็นเออย่างหนึ่งก็คือ pVAC (ของบริษัท InvivoGen) ซึ่งใช้ส่วน SV40 promoter
ความไม่เสถียรภาพของโครงสร้างดีเอ็นเอเป็นปัญหาสำคัญสำหรับผู้ผลิตพลาสมิด ของการฉีดวัคซีนดีเอ็นเอ และของการบำบัดด้วยยีน ส่วนต่าง ๆ ที่เป็นแกนหลัก (backbone) ของพลาสมิดอาจมีส่วนในการสร้างความไม่เสถียรภาพ รูปแบบลำดับยีนอันก่อความไม่เสถียรภาพที่รู้แล้วรวมทั้ง direct repeat, inverted repeat, tandem repeat ซึ่งพบใน cloning vector และ expression vector ที่มีขายทั่วไป ดังนั้น การลดหรือการกำจัดลำดับยีนภายในแกนหลักของพลาสมิดที่ไม่เข้ารหัสโปรตีนและไม่จำเป็น ก็จะลดโอกาสเกิดความไม่เสถียรภาพโดยตรง และดังนั้น ลดโอกาสการเกิดยีนรวมกันใหม่เนื่องกับพลาสมิด
กลไกของพลาสมิด
เมื่อพลาสมิดเข้าไปในนิวเคลียสของเซลล์แล้ว มันก็จะถอดรหัสเป็นเพปไทด์ซึ่งเป็นแอนติเจนแปลกปลอม โมเลกุลคอมเพล็กซ์ major histocompatibility complex (MHC) ทั้ง class I และ II ของเซลล์ก็จะนำแอนติเจนไปแสดงที่ผิวเซลล์ เซลล์ที่แสดงแอนติเจน (antigen-presenting cell) ก็จะเคลื่อนย้ายไปยังต่อมน้ำเหลือง แล้วแสดงแอนติเจนและโมเลกุลที่ช่วยกระตุ้น เป็นการส่งสัญญาณให้กับเซลล์ที แล้วเริ่มการตอบสนองของภูมิต้านทาน
รูปแบบโปรตีน/ดีเอ็นเอ
สารอิมมูโนเจนสามารถส่งเข้าไปยังส่วนโดยเฉพาะ ๆ ของเซลล์เพื่อเพิ่มการตอบสนองของแอนติบอดีหรือของเซลล์ทีที่ฆ่าเซลล์ (cytotoxic T-cell) แอนติเจนที่หลั่งออกหรือยึดอยู่กับเยื่อหุ้มเซลล์จะกระตุ้นการตอบสนองของแอนติบอดีได้ดีกว่าแอนติเจนที่อยู่ในไซโทซอล การตอบสนองของเซลล์ทีที่ฆ่าเซลล์อาจเพิ่มได้โดยปรับให้แอนติเจนสลายตัวในไซโทพลาซึมแล้วเข้าสู่กระบวนการส่งแอนติเจนไปที่ผิวเซลล์ของ major histocompatibility complex (MHC) class I ซึ่งปกติทำโดยเพิ่มยูบิควิติน (ubiquitin) ไปที่ยีนโปรตีนด้านเอ็น-เทอร์มินัส
คอนฟอร์เมชันของโปรตีนยังมีผลต่อการตอบสนองของแอนติบอดีอีกด้วย โครงสร้างที่เป็นระเบียบ (เช่น อนุภาคไวรัส) ได้ผลดีกว่าโครงสร้างอันไม่มีระเบียบมินิยีน (หรือ MHC class I epitopes) จากจุลชีพก่อโรคชนิดต่าง ๆ สามารถเพิ่มการตอบสนองของเซลล์ทีที่ฆ่าเซลล์เพื่อต่อต้านจุลชีพก่อโรคบางชนิด โดยเฉพาะเมื่อรวม epitope ชนิด TH เข้าไปด้วย
การส่งเข้าไปในเซลล์
มีวิธีส่งวัคซีนดีเอ็นเอเข้าไปในเนื้อเยื่อของสัตว์หลายอย่าง ในปี 1999 วิธียอดนิยมเมื่อฉีดวัคซีนดีเอ็นเอในน้ำเกลือก็คือ ใช้เข็มฉีดยาธรรมดา หรือใช้ปืนยิงยีน แต่หลังจากนั้นก็มีเทคนิคใหม่เพิ่มขึ้นเรื่อย ๆ
การฉีดดีเอ็นเอในน้ำเกลือ
วัคซีนดีเอ็นเอในน้ำเกลือปกติจะฉีดเข้ากล้ามเนื้อโครงร่าง หรือเข้าใต้ผิวหนัง เพื่อส่งดีเอ็นเอเข้าไปในร่างกายภายนอกเซลล์ ซึ่งสามารถช่วยด้วย
- กระบวนการ electroporation
- ทำใยกล้ามเนื้อให้เสียหายชั่วคราวด้วยพิษต่อกล้ามเนื้อ (myotoxin) เช่นยาชา bupivacaine
- ใช้สารละลายที่ความดันออสโมซิสสูงกว่าเลือด เช่น น้ำเกลือ หรือซูโครส
ภูมิคุ้มกันจะตอบสนองต่อวิธีนี้โดยขึ้นกับปัจจัยรวมทั้งชนิดเข็มฉีดยาที่ใช้ การวางเข็ม ฉีดเร็วแค่ไหน ปริมาณการฉีด ชนิดกล้ามเนื้อ อายุ เพศ และสภาพร่างกายของผู้รับวัคซีน
ปืนยิงยีน
ปืนยิงยีน (gene gun) สามารถยิงดีเอ็นเอในพลาสมิด (pDNA) โดยมีอนุภาคทองหรือทังสเตนอันดูดดีเอ็นเอเข้าไปเป็นลูกกระสุน ให้เข้าไปในเข้าไปในเซลล์ที่ต้องการ โดยใช้ฮีเลียมอัดเป็นตัวดันกระสุน
การส่งยาทางเยื่อบุ
วิธีการส่งยาทางอื่นรวมทั้งการฉีดยาพ่นเป็นดีเอ็นเอเปล่า (naked DNA) ที่ผิวเยื่อบุ/เยื่อเมือกต่าง ๆ เช่น ที่จมูก หรือที่ปอด ยาหยอดตา และยาทาช่องคลอด ยาที่ส่งผ่านเยื่อบุได้สำเร็จแล้วรวมทั้งชนิดที่ใช้ลิโปโซมหุ้มดีเอ็นเอโดยมีประจุบวก, ไมโครสเฟียร์ที่ย่อยสลายทางชีวภาพได้, เชื้อ Salmonella ลดฤทธิ์เป็นเวกเตอร์สำหรับส่งดีเอ็นเอทางปาก, เชื้อ Shigella หรือ Listeria เพื่อใช้เป็นเวกเตอร์ทางปากสำหรับเยื่อบุลำไส้ และเวกเตอร์อะดีโนไวรัสลูกผสม
ELI immunization
expression library immunization เป็นการสร้างเวกเตอร์ที่ได้โคลนยีนต่าง ๆ อันแสดงออกโปรตีนแต่ละชนิดของจุลชีพก่อโรคแล้วฉีดเป็นวัคซีน เมื่อใช้เทคนิคนี้ ก็อาจสามารถส่งยีนของจุลชีพทั้งหมดไปที่เซลล์ได้พร้อม ๆ กัน ซึ่งอาจมีประโยชน์สำหรับจุลชีพก่อโรคที่ลดฤทธิ์หรือเพาะได้ยาก วิธีนี้ยังสามารถใช้ระบุว่า ยีนตัวไหนของจุลชีพทำให้คุ้มกันตอบสนองแล้วป้องกันโรคได้ ซึ่งใช้ตรวจสอบอย่างสำเร็จแล้วกับแบคทีเรีย Mycoplasma pulmonis ซึ่งเป็นจุลชีพก่อโรคปอดที่มีจีโนมค่อนข้างเล็กในหนู แม้แต่ expression library ที่ไม่สมบูรณ์ก็ยังสามารถสร้างภูมิคุ้มกันได้
ตารางเปรียบเทียบ
| วิธีการส่ง | สูตรผสม | เนื้อเยื่อเป้าหมาย | ปริมาณดีเอ็นเอ | |
|---|---|---|---|---|
| การฉีดยา | ด้วยเข็มฉีดยา | สารละลายในน้ำเกลือ | เข้ากล้ามเนื้อโครงร่าง, เข้าชั้นผิวหนัง, (ส่วนการให้ผ่านเส้นลือดดำ, ฉีดเข้าชั้นใต้ผิวหนัง และฉีดเข้าช่องท้องจะได้ผลสำเร็จต่าง ๆ กัน) | ปริมาณมาก (ประมาณ 100-200 ไมโครกรัม) |
| ปืนยิงยีน | อนุภาคทองที่เคลือบด้วยดีเอ็นเอ | ที่หนังกำพร้าของท้อง, เยื่อบุช่องคลอด, ที่กล้ามเนื้อหรืออวัยวะอื่น ๆ ซึ่งเจาะให้เข้าถึงได้ | ปริมาณน้อย (อาจน้อยถึง 16 นาโนกรัม) | |
| การฉีดอัดแก๊ส (pneumatic) | สารละลาย | ที่หนังกำพร้า | ปริมาณมาก (อาจถึง 300 ไมโครกรัม) | |
| ยาทาภายนอก | สารละลาย | ตา ช่องคลอด | ปริมาณน้อย (ไม่เกิน 100 ไมโครกรัม) | |
| Cytofectin-mediated | ไลโปโซมมีประจุบวก, ไมโครสเฟียร์, เวกเตอร์อะดีโนไวรัสลูกผสม, เวกเตอร์ Shigella ที่ลดฤทธิ์แล้ว, วัคซีนแบบพ่นที่ประกอบด้วยลิพิดมีประจุบวก | ในกล้ามเนื้อ, ผ่านเส้นเลือดดำ (เพื่อให้เกิดผลที่เนื้อเยื่อทั่วร่างกาย), เข้าช่องท้อง, ยากินเพื่อให้เกิดผลที่เยื่อเมือกของลำไส้, ยาพ่นที่ให้เกิดผลที่เยื่อเมือกของจมูกหรือปอด | ต่าง ๆ กัน | |
| วิธี | ข้อดี | ข้อเสีย |
|---|---|---|
| การฉีดเข้ากล้ามเนื้อหรือเข้าหนัง |
|
|
| ปืนยิงยีน |
|
|
| การฉีดอัดแก๊ส |
|
|
| การส่งดีเอ็นเอที่อำนวยด้วยไลโปโซม |
|
|
ขนาดยา
วิธีการส่งยาเป็นตัวกำหนดขนาดยาที่ต้องใช้เพื่อให้เกิดภูมิต้านทานโรค การฉีดยาในน้ำเกลือจะต้องใช้ดีเอ็นเอปริมาณต่าง ๆ กัน เริ่มตั้งแต่ 10 ไมโครกรัมจนถึง 1 มิลลิกรัม เทียบกับการใช้ปืนยิงยีนที่ใช้น้อยกว่า 100-1,000 เท่า แม้ปกติแล้วต้องใช้ 0.2-20 ไมโครกรัม แต่ก็มีรายงานว่าใช้น้อยถึง 16 นาโนกรัมอยู่เหมือนกัน โดยจะต่าง ๆ กันขึ้นอยู่กับฉีดให้สัตว์ชนิดไหน ตัวอย่างเช่น หนูใช้ดีเอ็นเอประมาณ 10 เท่าน้อยกว่าไพรเมต การฉีดผสมน้ำเกลือต้องใช้ดีเอ็นเอมากกว่าเพราะส่งดีเอ็นเอเข้าไปยังบริเวณช่องว่างนอกเซลล์ของเนื้อเยื่อที่เป็นเป้า (ปกติจะเป็นกล้ามเนื้อ) แล้วต้องผ่านอุปสรรคต่าง ๆ (เช่น ชั้น basal lamina ของสารเคลือบเซลล์ และเนื้อเยื่อเกี่ยวพันจำนวนมาก) ก่อนที่จะเข้าไปในเซลล์ได้ เทียบกับปืนยิงยีนที่ยิงดีเอ็นเอเข้าไปในเซลล์โดยตรง จึงเสียดีเอ็นเอน้อยกว่า
การตอบสนองของภูมิคุ้มกัน
เซลล์ทีเฮลเปอร์
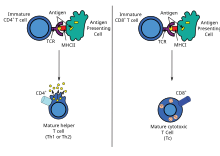
วัคซีนดีเอ็นเอก่อการตอบสนองของเซลล์ทีเฮลเปอร์ (TH) หลายรูปแบบรวมทั้งการเพิ่มเม็ดเลือดขาวอย่างรวดเร็ว (lymphoproliferation) และการตอบสนองทางไซโตไคน์ในรูปแบบต่าง ๆ ข้อดีเยี่ยมของวัคซีนดีเอ็นเอก็คือสามารถจัดให้ก่อการตอบสนองของเซลล์ทีชนิด TH1 หรือ TH2 ก็ได้ โดยวัคซีนแต่ละชนิดจะทำให้มีการตอบสนองโดยเฉพาะ ๆ ในเรื่องของการแสดงออก lymphokine กับ chemokine, สารภูมิต้านทาน, การขนส่งเม็ดเลือดขาว และการตอบสนองของระบบภูมิคุ้มกันโดยกำเนิด
การตอบสนองของเซลล์ทีอื่น ๆ
ชนิดของเซลล์ทีที่ตอบสนองจะขึ้นอยู่กับปัจจัยต่าง ๆ รวมทั้งการส่งวัคซีน ชนิดของอินมูโนเจนที่แสดงออก รวมถึงการส่งวัคซีนเข้าไปยังช่องต่าง ๆ ในต่อมน้ำเหลือง (lymphoid compartment) โดยเฉพาะ ๆ ทั่วไปแล้ว การฉีดผสมน้ำเกลือ (ไม่ว่าจะเข้าในกล้ามเนื้อหรือเข้าผิวหนัง) มักก่อการตอบสนองของเซลล์ทีชนิด TH1 และการใช้ปืนยิงยีนจะทำให้เซลล์ TH2 ตอบสนอง นี่เป็นจริงสำหรับแอนติเจนที่จับกับเยื่อหุ้มเซลล์และแอนติเจนในน้ำเลือด แต่ไม่จริงสำหรับแอนติเจนที่หลั่งออกมา ซึ่งมักจะก่อการตอบสนองของ TH2 ไม่ว่าจะส่งวัคซีนด้วยวิธีใด ๆ
ปกติแล้ว ชนิดเซลล์ทีที่ตอบสนองจะคงยืนเป็นระยะยาวโดยไม่เปลี่ยนไปเมื่อติดโรค หรือแม้เมื่อก่อภูมิคุ้มกันโดยวิธีที่ปกติจะทำให้เซลล์ทีอีกอย่างตอบสนองในบุคคลที่ไม่เคยติดโรคหรือไม่เคยได้วัคซีนมาก่อน แต่งานศึกษาปี 1995 ก็พบด้วยเหมือนกันว่าวัคซีนดีเอ็นเอที่เข้ารหัสโปรตีน circumsporozoite ของปรสิตมาลาเรียหนู คือ Plasmodium yoelii (ยีน PyCSP) เบื้องต้นทำให้เซลล์ TH2 ตอบสนอง แต่ต่อมาเปลี่ยนเป็น TH1 หลังได้วัคซีนโดสที่สอง
เหตุที่เซลล์ทีชนิดต่าง ๆ ตอบสนอง
มีเรื่องที่ยังไม่ชัดเจนหลายอย่างรวมทั้งกลไกของวิธีต่าง ๆ ตามที่ว่า, รูปแบบแอนติเจนที่แสดงออก และรูปแบบการตอบสนองของเซลล์ทีชนิดต่าง ๆ เบื้องแรกคาดว่า การฉีดเข้ากล้ามเนื้อที่ต้องใช้ดีเอ็นเอปริมาณมากเป็นเหตุให้เซลล์ทีแบบ TH1 ตอบสนอง แต่หลักฐานการทดลองกลับไม่แสดงว่าขนาดยามีผลต่อชนิดเซลล์ทีที่ตอบสนอง แต่ขึ้นอยู่กับการเปลี่ยนสภาพ (differentiation) ของเซลล์ที่แสดงแอนติเจนคือ antigen-presenting cell (APC) เซลล์เดนไดรต์ (dendritic cell ตัวย่อ DC) ซึ่งเป็น APC ชนิดหนึ่งอาจเปลี่ยนสภาพแล้วหลั่งอินเตอร์ลิวคินชนิด IL-12 ซึ่งสนับสนุนพัฒนาการของเซลล์ทีแบบ TH1 หรือหลั่งชนิด IL-4 ซึ่งสนับสนุนเซลล์แบบ TH2 คือ เมื่อใช้วิธีการฉีด pDNA เข้าไปในร่างกาย DC ก็จะกลืนมันเข้าไปผ่านกระบวนการเอนโดไซโทซิส ซึ่งจะกระตุ้นให้ให้เซลล์เปลี่ยนสภาพเพื่อผลิตไซโตไคน์ชนิด TH1 (คือ IL-12) เทียบกับปืนยิงยีนที่ส่งดีเอ็นเอเข้าไปในเซลล์โดยตรง จึงไม่กระตุ้น TH1 เยี่ยงนี้
ประโยชน์การทำให้เซลล์ทีโดยเฉพาะ ๆ ตอบสนองมากกว่า
การเกิดเซลล์ทีประเภทใดประเภทหนึ่งยิ่งกว่ามีประโยชน์ในเรื่องภูมิแพ้และโรคภูมิต้านตนเอง เมื่อมีโรคภูมิต้านตนเอง เป้าหมายการรักษาก็เพื่อเปลี่ยนการตอบสนองแบบ TH1 (คือเซลล์ทีซึ่งฆ่าเซลล์) ไปเป็นแบบ TH2 ซึ่งไม่ทำลายเซลล์ ซึ่งได้ประสบความสำเร็จแล้วในการชักนำ (priming) ให้เกิดการตอบสนองในรูปแบบที่ต้องการสำหรับสัตว์ทดลองพรีคลินิกในช่วงภาวะก่อนเกิดโรค (predisease) และได้ประสบความสำเร็จบ้างในการเปลี่ยนการตอบสนองสำหรับโรคที่เกิดแล้ว
การตอบสนองของเซลล์ทีชนิดทำลายเซลล์
ข้อดีอย่างหนึ่งของวัคซีนดีเอ็นเอก็คือสามารถทำให้เม็ดเลือดขาวชนิดทำลายเซลล์ (cytotoxic T lymphocyte, CTL) ตอบสนองโดยไม่มีความเสี่ยงเหมือนกับวัคซีนเชื้อเป็น การตอบสนองของ CTL สามารถเกิดกับเอพิโทปที่ CTL เข้าจับทั้งแบบ immunorecessive และ immunodominant ซึ่งคล้ายกับที่เกิดในการติดเชื้อตามธรรมชาติ ดังนั้น วัคซีนจึงอาจมีประโยชน์ในการตรวจสอบเอพิโทปที่ CTL เข้าจับและบทบาทของ CTL ในการสร้างภูมิคุ้มกัน
เซลล์ทีที่ฆ่าเซลล์สามารถรู้จำเพปไทด์ขนาดเล็ก (เป็นกรดอะมิโน 8-10 หน่วย) ที่เข้าคอมเพล็กซ์กับโมเลกุล MHC class I เป็นเพปไทด์อนุพัทธ์จากโปรตีนในไซโทซอลที่ได้สลายแล้วส่งไปให้โมเลกุล MHC class I ที่ยังใหม่ (nascent) ภายในร่างแหเอนโดพลาซึม (ER) การส่งผลิตภัณฑ์ยีนเข้าไปที่ ER โดยตรง (โดยสอดใส่ลำดับ ER insertion signal sequence ทางด้านเอ็น-เทอร์มินัส) สามารถเพิ่มการตอบสนองของ CTL ซึ่งประสบความสำเร็จแล้วกับไวรัสลูกผสม vaccinia ที่แสดงออกโปรตีนไข้หวัดใหญ่ โดยหลักการนี้ก็ควรจะใช้ได้กับวัคซีนดีเอ็นเอด้วย การจัดให้แอนติเจนเสื่อมภายในเซลล์ (และดังนั้น จึงสามารถเข้าไปในวิถีเมแทบอลิซึม MHC class I pathway) โดยเพิ่มยูบิควิตินซึ่งเป็นลำดับเพปไทด์ส่งสัญญาณ หรือโดยกลายพันธุ์ลำดับเพปไทด์ส่งสัญญาณอื่น ๆ พบว่ามีประสิทธิภาพเพิ่มการตอบสนองของ CTL การตอบสนองของ CTL ยังอาจเพิ่มได้ด้วยการฉีดโมเลกุลที่ร่วมกระตุ้น (co-stimulatory) วัคซีนดีเอ็นเอ โมเลกุลเช่น B7-1 หรือ B7-2 เพื่อต่อต้านนิวคลีโอโปรตีนของไข้หวัดใหญ่ หรือ GM-CSF เพื่อต่อต้านปรสิตมาลาเรีย Plasmodium yoelii ของหนู การฉีดวัคซีนดีเอ็นเอร่วมกับพลาดมิดที่เข้ารหัสโมเลกุลร่วมกระตุ้นเช่น IL-12 และ TCA3 พบว่าเพิ่มฤทธิ์ของ CTL ต่อแอนติเจนชนิดนิวคลีโอโปรตีนของ HIV-1 และไข้หวัดใหญ่
การตอบสนองทางน้ำเหลือง (สารภูมิต้านทาน)
การตอบสนองของแอนติบอดี/สารภูมิต้านทานที่วัคซีนดีเอ็นเอชักนำอาศัยปัจจัยหลายอย่างรวมทั้งชนิดของแอนติเจน แหล่งที่พบแอนติเจน (เช่น ในเซลล์หรือหลั่งออก) จำนวนโดส ความถี่ ขนาดวัคซีน ตำแหน่งที่ฉีด และวิธีการส่งแอนติเจน
จลนศาสตร์
การตอบสนองทางน้ำเหลืองเพราะฉีดวัคซีนดีเอ็นเอครั้งเดียวอาจมีผลที่คงยืนกว่าการฉีดวัคซีนโปรตีนลูกผสมครั้งเดียวเหมือนกัน ยกตัวอย่างเช่น การตอบสนองทางสารภูมิต้านทานต่อโปรตีนเปลือกหุ้ม (HBsAg) ของไวรัสตับอักเสบบี อาจคงยืนถึง 74 สัปดาห์โดยไม่ต้องฉีดบูสต์ อีกอย่างหนึ่ง ภูมิคุ้มกันตลอดชีวิตต่อต้านไกลโคโปรตีน haemagglutinin ของไข้หวัดใหญ่ก็ทำได้แล้วในหนูเมื่อใช้ปืนยิงยีน เซลล์ที่หลั่งสารภูมิต้านทาน (antibody-secreting cell, ASC) จะเคลื่อนไปยังไขกระดูกและม้ามแล้วสามารถสร้างสารภูมิต้านทานในระยะยาว โดยจะอยู่เป็นประจำที่นั่นหลังจากปีหนึ่ง
ตารางต่อไปจะแสดงการตอบสนองทางสารภูมิต้านทานเมื่อติดเชื้อไวรัสโดยธรรมชาติ, เมื่อสร้างภูมิคุ้มกันด้วยโปรตีนลูกผสม (recombinant protein) และด้วยวัคซีนดีเอ็นเอ วัคซีนดีเอ็นเอจะเพิ่มการตอบสนองทางสารภูมิต้านทานได้ช้ากว่าการติดเชื้อหรือโปรตีนลูกผสม โดยอาจต้องใช้เวลานานถึง 12 สัปดาห์ แต่การฉีดบูสต์ก็ลดช่วงเวลานี้ได้เหมือนกัน นี้น่าจะเป็นเพราะระดับแอนติเจนที่แสดงออกได้น้อยเป็นเวลาหลายอาทิตย์ ซึ่งต้องสนับสนุนการตอบสนองของสารภูมิต้านทานทั้งในระยะปฐมภูมิและทุติยภูมิ
มีการฉีดวัคซีนดีเอ็นเอที่แสดงออกโปรตีนเปลือก (envelope protein) ทั้งขนาดเล็กขนาดกลางของไวรัสตับอักเสบบีให้แก่ผู้ใหญ่ที่เป็นโรคตับอักเสบเรื้อรัง ซึ่งทำให้เซลล์ผลิตไซโตไคน์โดยเฉพาะ คือ interferon gamma อนึ่ง เซลล์ทีซึ่งรู้จักโปรตีนเปลือกหุ้มขนาดกลางก็เกิดขึ้นด้วย แต่การตอบสนองทางภูมิคุ้มกันของคนไข้ก็ยังไม่พอควบคุมการติดเชื้อไวรัสบี
| การเกิดภูมิคุ้มกัน | |||
|---|---|---|---|
| วัคซีนดีเอ็นเอ | วัคซีนโปรตีนลูกผสม | การติดเชื้อโดยธรรมชาติ | |
| ปริมาณแอนติเจนที่ใช้ | เป็นนาโนกรัม | เป็นไมโครกรัม | ? (นาโนกรัม-ไมโครกรัม) |
| ระยะที่แสดงแอนติเจน | เป็นอาทิตย์ ๆ | < 1 สัปดาห์ | หลายสัปดาห์ |
| จลนศาสตร์การเกิดแอนติบอดี | เพิ่มช้า | เพิ่มเร็ว | เพิ่มเร็ว |
| จำนวนครั้งที่ฉีด* | 1 | 2 | 1 |
| Ab isotype (สัตว์ตัวแบบเป็นหนู) | C’-dependent หรือ C’-independent | C’-dependent | C’-independent |
| *เพื่อให้ได้อิมมูโนโกลบูลินจีที่มี avidity สูงและให้เซลล์ที่หลั่งสารภูมิต้านทาน (ASC) ย้ายไปอยู่ที่ไขกระดูก | |||
อนึ่ง ความเข้มข้นของสารภูมิต้านที่วัคซีนดีเอ็นเอชักนำก็จะน้อยกว่าที่ได้จากโปรตีนลูกผสม แต่สารภูมิต้านทานเนื่องกับวัคซีนดีเอ็นเอมีสัมพรรคภาพ (affinity) กับเอพิโทปที่พับอยู่ในสภาพปกติ (native epitope) ที่แน่นกว่าสารภูมิต้านทานเนื่องกับโปรตีน กล่าวอีกนัยก็คือ วัคซีนดีเอ็นเอก่อการตอบสนองเชิงคุณภาพที่ดีกว่า โดยสารภูมิต้านทานจะเกิดด้วยการฉีดเพียงครั้งเดียว เทียบกับโปรตีนลูกผสมที่ต้องฉีดบูสต์ วัคซีนดีเอ็นเอยังสามารถก่อการตอบสนองของเซลล์ TH ในรูปแบบที่ต้องการ และดังนั้น จึงชักนำสารภูมิต้านทานใน isotype ที่ต้องการได้อีกด้วย ซึ่งไม่เกิดกับการติดเชื้อตามธรรมชาติหรือการฉีดโปรตีนเป็นวัคซีน
กลไกของภูมิคุ้มกันเนื่องกับดีเอ็นเอ
DNA uptake
เมื่อพบเป็นครั้งแรกว่า เซลล์กล้ามเนื้อในร่างกายดูดซึมดีเอ็นเอแล้วแสดงออกโปรตีน ตอนนั้นก็ยังคาดว่าเป็นเซลล์พิเศษเพราะมี T-tubule เป็นเครือข่ายขนาดใหญ่ ต่อมาเมื่อตรวจสอบด้วยกล้องจุลทรรศน์อิเล็กตรอนจึงเสนอว่า การดูดซึมดีเอ็นเอเข้าในเซลล์จะเกิดผ่านโครงสร้าง caveolae (หรือ non-clathrin coated pit) ที่เยื่อหุ้มเซลล์ แต่หลังจากนั้นกลับพบว่า เซลล์อื่น ๆ (เช่น keratinocyte, เซลล์สร้างเส้นใย และเซลล์เนื้อเยื่อบุผิวชนิดเซลล์ลังเกอร์ฮันส์) ก็สามารถนำดีเอ็นเอเข้าในเซลล์เหมือนกัน กลไกการนำดีเอ็นเอเข้าไปในเซลล์จึงยังไม่ชัดเจน
มีทฤษฎีหลักสองอย่าง คือ หนึ่ง เป็นการรับดีเอ็นเอเข้าไปอย่างไม่เฉพาะเจาะจง เช่น ดังที่พบในกระบวนการฟาโกไซโทซิสหรือพิโนไซโทซิส หรือ สอง เป็นการรับดีเอ็นเอเข้าไปผ่านหน่วยรับโดยเฉพาะ ๆ ซึ่งอาจรวม หน่วยรับที่ผิวเซลล์ขนาด 30 กิโลดัลตัน หรือหน่วยรับของแมคโครฟาจ หน่วยรับ 30 กิโลดัลตัน จะเข้ายึดอย่างเฉพาะเจาะจงกับส่วนดีเอ็นเอขนาด 4,500 bp (แล้วรับเข้าไปในเซลล์) โดยหน่วยรับพบอยู่ที่ antigen-presenting cell และเซลล์ที ส่วนหน่วยรับของแมคโครฟาจสามารถจับกับมาโครโมเลกุลหลายชนิด รวมทั้งโพลีไรโบนิวคลีโอไทด์ (polyribonucleotide) ซึ่งเป็นหน่วยโครงสร้างพื้นฐานของดีเอ็นเอและอาร์เอ็นเอ และดังนั้น จึงอาจเป็นตัวนำดีเอ็นเอเข้าไปในเซลล์ การดูดซึมดีเอ็นเอผ่านหน่วยรับอาจอำนวยโดยการมีลำดับยีนที่เป็นกัวนีนต่อ ๆ กัน (polyguanylate sequence) ในดีเอ็นเอ มีวิธีส่งวัคซีนอื่น ๆ ที่ไม่ส่งเข้าไปในเซลล์ผ่านกระบวนการเช่นนี้ เช่น ปืนยิงยีน และการส่งยีนโดยยึดไว้กับลิโปโซมเป็นต้น
การแสดงแอนติเจนของเซลล์
งานศึกษาต่าง ๆ กับหนูไคมีรา พบว่าเซลล์อนุพัทธ์จากเซลล์ไขกระดูกรวมทั้งเซลล์เดนไดรต์ แมคโครฟาจ และเซลล์บีที่ปรับตัวพิเศษ (specialized B cell) เป็นเซลล์แสดงแอนติเจนที่รวม ๆ เรียกว่า professional antigen presenting cellsเซลล์ลังเกอร์ฮันส์เป็นแมโครฟาจประจำเนื้อเยื่อผิวหนัง พบว่า หลังจากใช้ปืนยิงยีนเข้าที่ผิวหนัง เซลล์ลังเกอร์ฮันส์ที่ได้ดีเอ็นเอก็จะย้ายไปที่ต่อมน้ำเหลืองที่อยู่ใกล้ ๆ เพื่อแสดงแอนติเจน เทียบกับเมื่อฉีดวัคซีนในกล้ามเนื้อหรือในผิวหนัง จะเป็นเซลล์เดนไดรต์ที่ได้ดีเอ็นเอแล้วย้ายไปที่ต่อมน้ำเหลืองที่อยู่ใกล้ ๆ เพื่อแสดงแอนติเจน lj;oแมคโครฟาจที่ได้ดีเอ็นเออาจพบในเลือดที่เวียนไปในร่างกาย
นอกจากการส่งดีเอ็นเอเข้าไปในเซลล์เดนไดรต์และแมคโครฟาจโดยตรง (direct transfection) แล้ว ยังเกิดกระบวนการ cross priming เมื่อให้วัคซีนไม่ว่าจะโดยฉีดเข้ากล้ามเนื้อ เข้าผิวหนัง หรือผ่านปืนยิงยีน เมื่อเซลล์อนุพัทธ์ของเซลล์ไขกระดูกหนึ่งแสดงเพปไทด์ที่อีกเซลล์หนึ่งสังเคราะห์ขึ้นด้วย MHC class 1 กระบวนการนี้เรียกว่า cross priming ซึ่งเตรียมให้เซลล์ทีชนิดฆ่าเซลล์พร้อมในการตอบสนอง และดูจะสำคัญต่อความสมบูรณ์ในการตอบสนองทางภูมิคุ้มกันระยะปฐมภูมิ
เป้าหมาย
การฉีดวัคซีนเข้ากล้ามเนื้อและเข้าผิวหนังทำให้ภูมิคุ้มกันตอบสนองต่างกัน ที่ผิวหนัง เซลล์ประเภท keratinocyte, เซลล์สร้างเส้นใย และเซลล์ลังเกอร์ฮันส์ สามารถดูดซึมดีเอ็นเอแล้วแสดงแอนติเจนที่ชักนำให้เกิดการตอบสนองทางภูมิคุ้มกันในระยะปฐมภูมิ เซลล์ลังเกอร์ฮันส์ที่ได้ดีเอ็นเอจะย้ายออกจากผิวหนัง (ภายใน 12 ชม.) เข้าไปยังต่อมน้ำเหลืองใกล้ ๆ ที่ ๆ เซลล์อำนวยให้เซลล์บีและเซลล์ทีตอบสนอง ในกล้ามเนื้อโครงร่าง แม้เซลล์กล้ามเนื้อลายจะเป็นเซลล์ที่รับดีเอ็นเอเข้าไปมากที่สุด ก็กลับไม่สำคัญต่อการตอบสนองของภูมิคุ้มกัน แต่การฉีดดีเอ็นเอเข้ากล้ามเนื้อจะทะลักเข้าไปในต่อมน้ำเหลืองที่อยู่ใกล้ ๆ ภายในไม่กี่นาที แล้วเข้าไปในเซลล์เดนไดรต์ในที่นั้น ๆ แล้วก่อการตอบสนองของภูมิคุ้มกัน ส่วนเซลล์กล้ามเนื้อ (myocyte) ที่ได้รับดีเอ็นเอแล้วจะเป็นหน่วยเก็บแอนติเจนสำรองเพื่อให้เซลล์แสดงแอนติเจน (APC) นำไปแสดง
การตอบสนองของภูมิคุ้มกันที่คงยืน
วัคซีนดีเอ็นเอมีประสิทธิภาพสร้างความจำให้แก่ภูมิคุ้มกัน เพราะมีการแสดงคอมเพล็กซ์แอนติเจน-แอนติบอดีที่ follicular dendritic cells (FDC) ซึ่งช่วยกระตุ้นเซลล์บีอย่างมีกำลัง แอนติเจนที่เซลล์เดนไดรต์แสดงใน germinal center ของต่อมน้ำเหลือง ก็ยังช่วยกระตุ้นเซลล์ทีอีกด้วย FDC ช่วยให้ภูมิคุ้มกันเกิดความจำเพราะช่วงการผลิตแอนติบอดีจะคาบเกี่ยวกับการแสดงออกของแอนติเจนที่เป็นไปในระยะยาว จึงสามารถเกิดคอมเพล็กซ์แอนติเจน-แอนติบอดีที่ FDC แสดงได้
อินเตอร์เฟียรอน
ทั้งเซลล์ทีเฮลเปอร์และเซลล์ทีชนิดเป็นพิษต่อเซลล์ (cytotoxic T-cell) สามารถควบคุมการติดเชื้อไวรัสโดยหลั่งอินเตอร์เฟียรอน แม้เซลล์ทีชนิดเป็นพิษปกติจะฆ่าเซลล์ที่ติดเชื้อไวรัส แต่ก็สามารถระตุ้นให้หลั่งไซโตไคน์ต่อต้านไวรัสเช่น IFN-γ (interferon gamma) และ TNF-α (tumor necrosis factor alpha) ซึ่งไม่ฆ่าเซลล์แต่จำกัดการติดเชื้อไวรัสโดยลด (down-regulating) การแสดงออกองค์ประกอบของไวรัสได้ ดังนั้น วัคซีนดีเอ็นเอจึงสามารถใช้บรรเทาการติดเชื้อไวรัสอาศัยอินเตอร์เฟียรอนที่ไม่ทำลายเซลล์ ซึ่งได้พิสูจน์แล้วกับเชื้อไวรัสตับอักเสบบี อนึ่ง IFN-γ เป็นโปรตีนส่งสัญญาณซึ่งสำคัญยิ่งในการควบคุมการติดเชื้อมาลาเรีย จึงมีลู่ทางว่าอาจใช้ทำวัคซีนดีเอ็นเอต้านมาลาเรียได้
การปรับการตอบสนองของภูมิคุ้มกัน
ดูเพิ่ม
แหล่งข้อมูลอื่น
- Hooper, JW; Thompson, E; Wilhelmsen, C; Zimmerman, M; Ichou, MA; Steffen, SE; Schmaljohn, CS; Schmaljohn, AL; Jahrling, PB (May 2004). "Smallpox DNA vaccine protects nonhuman primates against lethal monkeypox". Journal of Virology. 78 (9): 4433–43. doi:10.1128/JVI.78.9.4433-4443.2004. PMC 387704. PMID 15078924.
| การพัฒนา | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| กลุ่ม | |||||||||||
| การจัดการ |
|
||||||||||
| วัคซีน |
|
||||||||||
| เรื่องโต้แย้ง | |||||||||||
| บทความที่สัมพันธ์กัน | |||||||||||