
ฟาวิพิราเวียร์
| ฟาวิพิราเวียร์ | |
|---|---|
| |
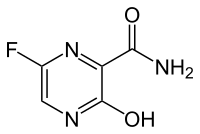
| ชื่อตาม IUPAC | 5-Fluoro-2-hydroxypyrazine-3-carboxamide |
| ชื่ออื่น | T-705; Avigan |
| เลขทะเบียน | |
| เลขทะเบียน CAS | 259793-96-9 |
| PubChem | 492405 |
| SMILES |
|
| InChI |
|
| ChemSpider ID | 431002 |
| คุณสมบัติ | |
| สูตรโมเลกุล | C5H4FN3O2 |
| มวลโมเลกุล | 157.1 g mol−1 |
| หากมิได้ระบุเป็นอื่น ข้อมูลข้างต้นนี้คือข้อมูลสาร ณ ภาวะมาตรฐานที่ 25 °C, 100 kPa | |
| สถานีย่อย:เคมี | |
ฟาวิพิราเวียร์ (Favipiravir) หรือที่รู้จักกันในชื่อ T-705 หรือ Avigan เป็นยาต้านไวรัสที่พัฒนาโดยบริษัทโตยามะเคมิคอล (富山化学工業) ของประเทศญี่ปุ่น มีฤทธิ์ต่อต้านอาร์เอ็นเอไวรัสหลายชนิด ในเดือนกุมภาพันธ์ พ.ศ. 2563 ได้รับการศึกษาแบบสุ่มในประเทศจีนเพื่อทำการทดลองรักษาโรค COVID-19 (โรคติดเชื้อโคโรนาไวรัส 2019) ที่พึ่งอุบัติขึ้น ฟาวิพิราเวียร์ ได้รับการรับรองระยะสั้นเป็นเวลาห้าปี เมื่อวันที่ 16 กุมภาพันธ์ พ.ศ. 2563 ในฐานะยาต้านไวรัสที่มีประสิทธิภาพต่อต้านโรค และในตอนนี้ได้ผลิตในประเทศจีนภายใต้ชื่อ ฟาวิลาเวียร์ (Favilavir) เช่นเดียวกับยาต้านไวรัสทดลองอื่น ๆ (T-1105 และ T-1106) ฟาวิพิราเวียร์เป็นอนุพันธ์ของ ไพราซีนคาร์โบซาไมด์ (Pyrazinecarboxamide) และยังมีฤทธิ์ต้านไวรัสไข้หวัดใหญ่, ไวรัสเวสต์ไนล์, ไวรัสไข้เหลือง, ไวรัสโรคปากและเท้า รวมถึงเชื้อไวรัสอื่น ๆ ในตระกูลฟลาวิไวรัส (Flaviviruses), อรีนาไวรัส (Arenaviruses), บุนยาไวรัส (Bunyaviruses) และ อัลฟาไวรัส (Alphaviruses) ฤทธิ์ในการต่อต้านเอนเทอโรไวรัส (Enteroviruses) และไวรัสโรคไข้ริฟต์แวลลีย์ ก็แสดงให้เห็นเช่นกัน ฟาวิพิราเวียร์ แสดงประสิทธิภาพอย่างจำกัดต่อไวรัสซิกาในการศึกษาในสัตว์ แต่มีประสิทธิภาพน้อยกว่ายาต้านไวรัสชนิดอื่นเช่น MK-608 และยังแสดงให้เห็นถึงประสิทธิภาพบางอย่างในการต่อต้านโรคพิษสุนัขบ้า ซึ่งได้ถูกนำมาใช้ในการทดลองในมนุษย์บางคนที่ติดเชื้อไวรัสดังกล่าว
กลไกการออกฤทธิ์นั้นเชื่อกันว่าเกี่ยวข้องกับการยับยั้งการคัดเลือกเอนไซม์ อาร์เอ็นเอโพลิเมอเรสที่ขึ้นกับอาร์เอ็นเอของไวรัส (RNA-dependent RNA polymerase) งานวิจัยอื่น ๆ แสดงให้เห็นว่า ฟาวิพิราเวียร์ ชักนำให้เกิดการกลายพันธุ์ในอาร์เอ็นเอที่ทำให้เกิดการตาย ซึ่งผลทำให้ฟีโนไทป์ของไวรัสไม่อาจมีชีวิตอยู่ได้ ฟาวิพิราเวียร์ เป็นโปร-ดรัก (prodrug) ที่ถูกกระบวนการเมตาบอลิซึมเผาผลาญไปเป็นรูปแบบที่ออกฤทธิ์คือ Favipiravir-ribofuranosyl-5'-triphosphate (Favipiravir-RTP) มีทั้งที่อยู่ในตำรับที่ให้โดยทางรับประทานและทางหลอดเลือดดำ เอ็นไซม์ Human hypoxanthine guanine phosphoribosyltransferase (HGPRT) เชื่อว่ามีบทบาทสำคัญในกระบวนการกระตุ้นการออกฤทธิ์นี้ ฟาวิพิราเวียร์ ไม่ยับยั้งการสังเคราะห์อาร์เอ็นเอหรือดีเอ็นเอ ในเซลล์ของสัตว์เลี้ยงลูกด้วยนมและไม่เป็นพิษต่อเซลล์ ในปี พ.ศ. 2557 ฟาวิพิราเวียร์ได้รับการอนุมัติในประเทศญี่ปุ่นสำหรับการสำรองยาต่อต้านการระบาดทั่วของโรคไข้หวัดใหญ่ อย่างไรก็ตาม ฟาวิพิราเวียร์ยังไม่ได้แสดงว่ามีประสิทธิภาพในเซลล์เยื่อบุทางเดินหายใจปฐมภูมิของมนุษย์ เป็นเหตุให้ยังมีความสงสัยในประสิทธิภาพในการรักษาโรคไข้หวัดใหญ่
กรณีโรคไวรัสอีโบลา
ยาดูเหมือนจะมีประสิทธิภาพในตัวอย่างของโรคไวรัสอีโบลาในหนู แต่ประสิทธิภาพของยาต้านการติดเชื้ออีโบลาในมนุษย์นั้นไม่ได้รับการพิสูจน์ ในช่วงการระบาดของไวรัสอีโบลาในแอฟริกาตะวันตกปี พ.ศ. 2557 มีรายงานว่าพยาบาลชาวฝรั่งเศสคนหนึ่งซึ่งติดเชื้ออีโบลาในขณะที่เป็นอาสาสมัครขององค์การแพทย์ไร้พรมแดน (MSF) ในไลบีเรียฟื้นตัวจากโรคหลังจากได้รับ ฟาวิพิราเวียร์การทดลองทางคลินิกที่ตรวจสอบการใช้ฟาวิพิราเวียร์ กับโรคไวรัสอีโบลาเริ่มต้นขึ้นในเมืองเกกเกดู (Guéckédou) ประเทศกินี ระหว่างเดือนธันวาคม พ.ศ. 2557 ผลเบื้องต้นแสดงให้เห็นว่าอัตราการตายลดลง ในผู้ป่วยที่มีเชื้อไวรัสอีโบลาในกระแสเลือดในระดับต่ำถึงปานกลาง แต่ไม่มีผลต่อผู้ป่วยที่ติดเชื้อไวรัสในระดับสูง ซึ่งเป็นกลุ่มที่มีความเสี่ยงสูงต่อการเสียชีวิต การออกแบบการทดลองได้รับการวิพากษ์วิจารณ์จากสก็อตต์ แฮมเมอร์ (Scott Hammer) และคนอื่น ๆ จากการใช้เพียงประวัติในการควบคุมโรคเท่านั้น ผลของการทดลองทางคลินิกนี้ได้ถูกนำเสนอโดยดาอูดา ซิสโซโก (Daouda Sissoko) ในเดือนกุมภาพันธ์ พ.ศ. 2559 ณ การประชุมประจำปีเกี่ยวกับรีโทรไวรัสและการติดเชื้อฉวยโอกาส (CROI) และเผยแพร่เมื่อวันที่ 1 มีนาคม พ.ศ. 2559 ในวารสารทางการแพทย์ PLOS Medicine
การประยุกต์ใช้กับโรคติดเชื้อโคโรนาไวรัส 2019 (COVID-19)
ในช่วงต้นเดือนกุมภาพันธ์ พ.ศ. 2563 มีการคาดการณ์ว่าฟาริพิราเวียร์น่าจะมีผลต่อต้านโคโรนาไวรัสสายพันธุ์ใหม่ (SARS-CoV-2) ได้
จากเอกสารฉบับร่างซึ่งตีพิมพ์ในเอกสารรายงานวิชาการ Nature Cell Biology โดยคณะนักวิจัยจากสถาบันวิจัยไวรัสแห่งอู่ฮั่นภายใต้สถาบันวิทยาศาสตร์แห่งประเทศจีน ในวันที่ 4 กุมภาพันธ์ พ.ศ. 2563 จากการวิจัยในหลอดทดลองโดยใช้เซลล์มาตรฐานที่แยกจากเซลล์เยื่อบุผิวไตที่สกัดจากลิงเวอร์เว็ท (Vero E6) ผลการประเมินการทดสอบสารต้านไวรัส SARS-CoV-2 จำนวนเจ็ดชนิดรวมถึง ฟาวิพิราเวียร์ซึ่งรายงานผลเป็นค่า 50% Effective concentration (EC50) ซึ่งฟาวิพิราเวียร์ให้ค่า 61.88 μM (ไมโครโมล/ลิตร) ในขณะที่ เรมเดซิเวียร์ซึ่งถูกพัฒนาขึ้นเพื่อใช้ในการรักษาโรคไข้เลือดออกอีโบลา มีค่า EC50 0.77 μM (ไมโครโมล/ลิตร) ซึ่งแสดงถึงประสิทธิภาพที่ดีกว่าฟาริพิราเวียร์ถึง 80 เท่า และยาต้านไข้มาลาเรีย คลอโรควิน ให้ค่า EC50 1.13 μM (ไมโครโมล/ลิตร) มีประสิทธิภาพมากเป็นอันดับสองจากสารทดลองทั้งเจ็ด อย่างไรก็ตามเมื่อพิจารณาค่า EC50 ของฟาริพิราเวียร์เมื่อทดสอบกับไวรัสอีโบลามีค่า 67 μM (ไมโครโมล/ลิตร) และยังแสดงผลการต้านไวรัสอีโบลาที่ดีมากในการทดลองในสิ่งมีชีวิตทั้งการทดสอบทางคลินิก และผลในสัตว์ทดลอง ซึ่งในกรณีเดียวกัน เรมเดซิเวียร์ ไม่แสดงผลที่มีนัยสำคัญ จากเหตุดังกล่าว คณะวิจัยจึงสรุปให้มีการทดสอบฟาริพิราเวียร์ในสิ่งมีชีวิตต่อไป
วันที่ 15 กุมภาพันธ์ พ.ศ. 2563 จากการตีพิมพ์ในหนังสือพิมพ์ เคอจี่รื่อเป้า (科技日报) ซึ่งเผยแพร่โดยกระทรวงวิทยาศาสตร์และเทคโนโลยีของสาธารณรัฐประชาชนจีน จากข้อสรุปผลการทดลองในหลอดทดลองข้างต้น การทดลองทางคลินิกได้เริ่มดำเนินการแล้วในสาธารณรัฐประชาชนจีน โดยดำเนินการให้ยาฟาริพิราเวียร์ในผู้ป่วย 70 ราย (รวมถึงกลุ่มควบคุมที่ได้รับยาหลอก) และได้แสดงผลการรักษาที่ชัดเจนมีอาการไม่พึงประสงค์จากยาที่ต่ำเพียงพอในระยะแรก ในกลุ่มที่ได้รับการรักษาอัตราการกำจัดกรดนิวคลีอิกของไวรัสสูงกว่ากลุ่มควบคุมอย่างมีนัยสำคัญ ใน 3 ถึง 4 วันหลังเริ่มการทดลอง (ผลของ เรมเดซิเวียร์ และคลอโรควิน ไม่ได้กล่าวถึงในบทความ)
นอกจากนี้บทความในหนังสือพิมพ์ เคอจี่รื่อเป้า ฉบับวันที่ 13 กุมภาพันธ์ พ.ศ. 2563 มีข้อมูลเกี่ยวกับผลกระทบทางคลินิกที่ค่อนข้างเฉพาะเช่น จากการให้สัมภาษณ์กลุ่มการวิจัยทางคลินิกได้ทำการศึกษา 26 ตัวอย่างที่โรงพยาบาลประชาชนที่สามเชินเจิ้น (深圳市第三人民医院) ในจำนวนนี้ผู้ป่วย 25 คน มีความรุนแรงของโรคปานกลางและ 25 คนมีอาการหนัก ฟาริพิราเวียร์ไม่มีผลข้างเคียงที่ชัดเจน มีการยอมรับของผู้ป่วยที่ดี มีผลลดไข้ที่ค่อนข้างดีในผู้ป่วยที่มีไข้ โดยหลังจากได้รับยา 2 วัน 72% มีไข้ลดลง และในสามวันผู้ป่วย 38% มีผลภาพรังสีปอดที่ดีขึ้น และดีขึ้นเป็น 70% ภายใน 6 วัน
เมื่อวันที่ 17 กุมภาพันธ์ พ.ศ. 2563 เหตุผลที่ฟาริพิราเวียร์ แสดงออกถึงผลที่ดีในการทดลองทางคลินิกในสิ่งมีชีวิต แม้จะมีผลน้อยกว่าเรมเดซิเวียร์ และคลอโรควิน ในสภาพแวดล้อมในหลอดแก้ว ได้รับการอธิบายโดย จง อู่ (钟武) หนึ่งในคณะวิจัยที่ตีพิมพ์บทความเมื่อวันที่ 4 กุมภาพันธ์ว่า "ฟาริพิราเวียร์ เป็นสารยับยั้งเอนไซม์อาร์เอ็นเอพอลิเมอเรส แต่ขณะเดียวกันก็เป็น โปร-ดัก และต้องการกระบวนการ Tri-phosphorylation ในสิ่งมีชีวิตเพื่อสร้างสารตั้งต้นแข่งขันเข้าทำปฏิกริยากับเอนไซม์อาร์เอ็นเอพอลิเมอเรส" ในการทดสอบในหลอดทดลอง กระบวนการ Tri-phosphorylation มีไม่เพียงพอ ซึ่งมีผลกระทบต่อผลการทดลองที่แสดงออกมา
จากการรายงานของสำนักข่าวซินหัว ในวันที่ 21 กุมภาพันธ์ พ.ศ. 2563 มีการทดลองยาฟาพิลาเวียร์ (Fapilavir - ชื่อในประเทศจีน) ในผู้ป่วย 80 กรณีในเชินเจิ้น ซึ่งข้อมูลจำนวนกรณีของการทดลองค่อนข้างสับสน
บริษัท เจ้อเจียงไห่เจิ้ง ฟาร์มาซูติคอล (浙江海正薬业股份有限公司) ได้รับการอนุมัติใบอนุญาตในการผลิตจากสำนักงานคณะกรรมการอาหารและยาแห่งชาติจีน (国家薬监局) ในวันที่ 16 กุมภาพันธ์ พ.ศ. 2563 และพร้อมที่จะผลิตและเริ่มจำหน่ายยาในชื่อฟาวิลาเวียร์ (Favilavir)
ในวันที่ 22 กุมภาพันธ์ พ.ศ. 2563 รัฐบาลญี่ปุ่นตัดสินใจที่จะให้มีการใช้ยา Avigan สำหรับผู้ติดเชื้อไวรัส SARS-CoV-2 และมีรายงานว่า บริษัทยาจำเป็นต้องเพิ่มการผลิตในไม่ช้า ในวันเดียวกันนั้นรัฐมนตรีว่าการกระทรวงสาธารณสุขแรงงานและสวัสดิการ คัตสึโนบุ คาโต ได้เปิดเผยว่าการสั่งจ่ายยาให้กับผู้ป่วยได้เริ่มขึ้นแล้ว
การใช้ยา
โดยทั่วไปสำหรับผู้ใหญ่โดยขนาดการรับประทาน 1,600 มิลลิกรัม วันละสองครั้งในวันแรก และ 600 มิลลิกรัม วันละสองครั้งในวันที่ 2 ถึงวันที่ 5 ระยะเวลาการรักษาโดยรวมคือ 5 วัน ด้วยยาเม็ดขนาด 200 มิลลิกรัม ดังนั้นจึงต้องรับประทาน (1600 x 2 + 600 x 2 x 4) มก. / 200 มก. = 40 เม็ดต่อคน ผลจากการได้รับยาในปริมาณสูงยังคงอยู่ระหว่างการศึกษา
ความเป็นพิษต่อทารกในครรภ์ ได้รับการยืนยันในการศึกษาในสัตว์ทดลอง และมีข้อห้ามใช้ยาในหญิงตั้งครรภ์และหญิงที่สงสัยว่าตั้งครรภ์ และควรคุมกำเนิดในช่วงเวลาระหว่างได้รับยาจนถึง 7 วันภายหลัง
ดูเพิ่ม
เชิงอรรถ
| ไวรัสตับอักเสบซี |
|
||||||||
|---|---|---|---|---|---|---|---|---|---|
| พิคอร์นาไวรัส | |||||||||
| ไวรัสไข้หวัดใหญ่ | |||||||||
| หลายกลไก/ทั่วไป |
|
||||||||