ยาปฏิชีวนะ
| ยาปฏิชีวนะ | |
|---|---|
| ระดับชั้นของยา | |
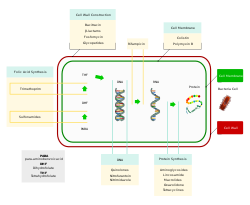
 การทดสอบความไวของแบคทีเรีย Staphylococcus aureus ต่อยาปฏิชีวนะด้วยวิธี Kirby-Bauer disk diffusion method โดยยาปฏิชีวนะจะกระจายเข้าไปในจานเพาะเลี้ยงที่มีเชื้อแบคทีเรียอยู่และส่งผลยับยั้งการเจริญเติบโตของ S. aureus ทำให้เกิดวงยับยั้งเชื้อ (Zone of inhibition) ขึ้น
| |
| In Wikidata |

ยาปฏิชีวนะ (อังกฤษ: antibiotic จากภาษากรีกโบราณ αντιβιοτικά, antiviotika) หรือเรียกอีกชื่อหนึ่งว่า ยาฆ่าเชื้อแบคทีเรีย (antibacterial) เป็นกลุ่มย่อยของยาอีกกลุ่มหนึ่งในกลุ่มยาต้านจุลชีพ (antimicrobial drugs) ซึ่งเป็นยาที่ถูกใช้ในการรักษาและป้องกันการติดเชื้อแบคทีเรีย โดยอาจออกฤทธิ์ฆ่าหรือยับยั้งการเจริญเติบโตของแบคทีเรียอย่างใดอย่างหนึ่งหรือทั้งสอง ยาปฏิชีวนะบางชนิดอาจมีคุณสมบัติเป็นมีคุณสมบัติเป็นสารต้านโพรโทซัวได้ เช่น เมโทรนิดาโซล ทั้งนี้ ยาปฏิชีวนะไม่มีฤทธิ์ในการต้านไวรัสที่เป็นสาเหตุของโรคต่าง ๆ เช่น ไข้หวัด หรือ ไข้หวัดใหญ่ เป็นต้น โดยยาที่มีฤทธิ์ต่อเชื้อไวรัสจะถูกจัดอยู่ในกลุ่มยาต้านไวรัส ซึ่งเป็นกลุ่มย่อยอีกกลุ่มหนึ่งของยาต้านจุลชีพ
ในบางครั้ง คำว่า ยาปฏิชีวนะ (ซึ่งหมายถึง "การต่อต้านชีวิต") ถูกนำมาใช้เพื่อสื่อความถึงสารใด ๆ ที่นำมาใช้เพื่อต้านจุลินทรีย์ ซึ่งมีความหมายเดียวกันกับคำว่า ยาต้านจุลชีพ บางแหล่งมีการใช้คำว่า ยาปฏิชีวนะ และ ยาฆ่าเชื้อแบคทีเรีย ในความหมายที่แยกจากกันไป โดยคำว่า ยา (สาร) ฆ่าเชื้อแบคทีเรีย จะสื่อความถึง สบู่ และน้ำยาฆ่าเชื้อ ขณะที่คำว่า ยาปฏิชีวนะ จะหมายถึงยาที่ใช้ในทางการแพทย์เพื่อฆ่าเชื้อแบคทีเรีย
การพัฒนายาปฏิชีวนะเริ่มต้นในช่วงศตวรรษที่ 20 พร้อมกับการพัฒนาเรื่องการให้วัคซีนเพื่อป้องกันโรคจากเชื้อจุลชีพต่าง ๆ การเกิดขึ้นของยาปฏิชีวนะนำมาซึ่งการกำจัดโรคติดเชื้อแบคทีเรียต่าง ๆ ออกไปหลายชนิด เช่น กรณีของวัณโรคที่ระบาดในประเทศกำลังพัฒนา อย่างไรก็ตาม ด้วยประสิทธิภาพที่ดีและการเข้าถึงยาที่ง่ายนำไปสู่การใช้ยาปฏิชีวนะในทางที่ผิด พร้อม ๆ กับการที่แบคทีเรียมีการพัฒนาจนกลายพันธุ์เป็นเชื้อแบคทีเรียที่ดื้อต่อยาปฏิชีวนะ ปัญหาดังข้างต้นได้แพร่กระจายเป็นวงกว้าง จนเป็นปัญหาสำคัญของการสาธารณสุขในทุกประเทศทั่วโลก จนองค์การอนามัยโลก (World Health Organization) ได้ประกาศให้ปัญหาการดื้อยาของเชื้อแบคทีเรียเป็น "ปัญหาสำคัญเร่งด่วนที่สุดที่เกิดขึ้นในทุกภูมิภาคทั่วโลกและทุกคนล้วนจะต้องได้รับผลกระทบจากปัญหานี้ ไม่ว่าวัยใด หรือประเทศใดก็ตาม"
ศัพทมูลวิทยา

คำว่า 'antibiosis' ซึ่งมีความหมายว่า "ต่อต้านชีวิต" ถูกนำมาใช้เป็นครั้งแรกโดยนักจุลชีววิทยาชาวฝรั่งเศส ฌอง ปอล วูยล์ลีแม็ง (Jean Paul Vuillemin) เพื่ออธิบายปรากฏการณ์การออกฤทธิ์ต้านเซลล์สิ่งมีชีวิตของยาปฏิชีวนะที่ถูกค้นพบในช่วงแรก ทั้งนี้ได้มีการอธิบายปรากฏการณ์การเกิด 'antibiosis' ในแบคทีเรียขึ้นเป็นครั้งแรกในปี ค.ศ. 1877 เมื่อ หลุยส์ ปาสเตอร์ และ โรเบิร์ต คอค พบว่าแบคทีเรียสกุลบาซิลลัสในอากาศสามารถยับยั้งการเจริญเติบโตของแบคทีเรีย Bacillus anthracis ได้ ซึ่งต่อมาคำดังกล่าวได้ถูกเปลี่ยนเป็น 'antibiotic' โดย เซลมัน แวกส์มัน – นักจุลชีววิทยาชาวอเมริกัน เมื่อ ค.ศ. 1942
คำว่า antibiotic นั้นปรากฏเป็นครั้งแรกในบทความวารสารทางการแพทย์ใน ปี ค.ศ. 1942 โดย เซลมัน แวกส์มัน และทีมนักวิจัยของเขา เพื่อใช้สื่อถึงสารที่มีความเจือจางสูงชนิดใด ๆ ที่จุลชีพสายพันธุ์หนึ่ง ๆ สร้างขึ้นเพื่อต่อต้านหรือยับยั้งการเจริญเติบโตของจุลชีพสายพันธุ์อื่น ซึ่งนิยามนี้จะไม่รวมสารที่ออกฤทธิ์ฆ่าแบคทีเรียแต่ไม่ได้ถูกสร้างขึ้นโดยจุลชีพ (เช่น น้ำย่อย และไฮโดรเจนเพอร์ออกไซด์) รวมไปถึงสารประกอบที่สังเคราะห์เลียนแบบสารที่ได้จากแบคทีเรีย เช่น ยากลุ่มซัลโฟนาไมด์ ในการนิยามความหายของคำว่า antibiotic หรือยาปฏิชีวนะในปัจจุบันนั้น จะหมายความรวมไปถึงยาใด ๆ ก็ตามที่ออกฤทธิ์ฆ่าหรือยับยั้งการเจริญเติบโตของแบคทีเรีย ไม่ว่ายานั้น ๆ จะถูกสร้างจากจุลชีพหรือไม่ก็ตาม
คำว่า "antibiotic" นั้นมีรากศัพท์จากคำ 2 คำ คือ anti ซึ่งมีความหมายว่า ต่อต้าน กับ βιωτικός (biōtikos) ที่มีความหายว่า "เหมาะกับชีวิต, มีชีวิต" ซึ่งคำว่า βιωτικός นั้นก็เกิดจากคำ 2 คำ คือ βίωσις (biōsis) ที่แปลว่า "หนทางแห่งชีวิต"และคำว่า βίος (bios) ที่หมายถึง "ชีวิต" ส่วนอีกคำหนึ่งให้ความหมายเหมือน "antibiotic" คือคำว่า "antibacterial" ซึ่งมาจากภาษากรีก ἀντί (anti) ที่มีความหมายว่า "ต่อต้าน" กับคำว่า βακτήριον (baktērion) ซึ่งแผลงมาจากคำว่า βακτηρία (baktēria) ซึ่งมีความหมายว่า "พลอง, กระป๋อง" ทั้งนี้ เนื่องจากแบคทีเรียสายพันธุ์แรกที่ถูกค้นพบนั้นมีรูปร่างเป็นแท่งคล้ายรูปทรงของพลองหรือกระป๋อง
ประวัติและการค้นพบ
การสกัดยาปฏิชีวนะจากรา
สารที่มีคุณสมบัติเป็นยาปฏิชีวนะนั้นถูกนำมาใช้ด้วยวัตถุประสงค์ที่หลากหลายนับตั้งแต่สมัยโบราณ ในช่วงก่อนคริสต์ศตวรรษที่ 20 การรักษาโรคติดเชื้อนั้นจะใช้ยาแผนโบราณเป็นหลัก โดยปรากฏมีการนำยาน้ำมิกซ์เจอร์ (Mixtures) ที่มีคุณสมบัติในการต้านจุลชีพมาใช้ในการรักษาโรคติดเชื้อเป็นเวลามากกว่า 2000 ปีที่แล้ว อารยธรรมโบราณหลายแห่ง รวมถึงอียิปต์โบราณ และกรีซโบราณ มีการนำส่วนผสมหรือสารสกัดจากราและพืชสายพันธุ์ที่จำเพาะมารักษาโรคติดเชื้อชนิดต่าง ๆ ส่วนการทดลองศึกษาในยุคถัดมานั้นมักทำขึ้นในห้องปฏิบัติการเพื่อทดลองและเฝ้าสังเกตการสังเคราะห์สารเพื่อต่อต้านซึ่งกันและกันในจุลชีพที่ต่างสายพันธ์กัน จนนำไปสู่การค้นพบยาต้านแบคทีเรียจากธรรมชาติที่สร้างจากจุลชีพในที่สุด หลุยส์ ปาสเตอร์ ได้ให้ข้อคิดเห็นและตั้งข้อสังเกตไว้ว่า "หากเราสามารถเข้าใจการต้านกันและกันระหว่างเชื้อแบคทีเรียบางชนิดได้ นั่นก็จะเป็นความหวังที่ยิ่งใหญ่ที่สุดสำหรับการรักษาโรคติดเชื้อ"
ใน ค.ศ. 1874 นักฟิสิกส์ชาวเวลล์นามว่า เซอร์วิลเลียม โรเบิตส์ (Sir William Roberts) ได้เขียนบันทึกไว้ว่า ราสายพันธุ์ Penicillium glaucum ที่ใช้ในการผลิตเนยแข็งสีน้ำเงินบางชนิดนั้นไม่มีการปนเปื้อนของแบคทีเรียเลย ต่อมาในปี 1876 จอห์น ทินดอลล์ (John Tyndall) – นักฟิสิกส์ชาวอังกฤษสันนิษฐานว่าราสกุลดังกล่าวนั้นอาจมีการผลิตสารบางชนิดที่ส่งผลยับยั้งการเจริญเติบโตของแบคทีเรียได้ ซึ่งต่อมาปาสเตอร์ได้ทำการศึกษาประเด็นดังกล่าวและพบว่า แบคทีเรียสายพันธุ์ Bacillus anthracis นั้นจะไม่เจริญเติบโตในสภาวะที่มีราสายพันธุ์ Penicillium notatum อยู่
ใน ค.ศ. 1895 วินเซนโซ ติเบริโอ (Vincenzo Tiberio) – นักฟิสิกส์ชาวอิตาลี ได้ตีพิมพ์บทความทางวารสารที่มีเนื้อหาเกี่ยวกับประสิทธิภาพในการต้านแบคทีเรียของสารสกัดจากราบางสายพันธุ์ ต่อมา ค.ศ. 1897 นักเรียนแพทย์ชาวฝรั่งเศส เออร์เนสต์ ดูเชส (Ernest Duchesne) ได้เสนอวิทยานิพนธ์เรื่อง "Contribution à l'étude de la concurrence vitale chez les micro-organismes: antagonisme entre les moisissures et les microbes" (การมีส่วนร่วมในการศึกษาเกี่ยวกับการแข่งขันที่เกี่ยวเนื่องกับชีวิตในจุลินทรีย์: การต้านกันของราและจุลชีพ) ซึ่งถือเป็นนักวิชาการคนแรกที่พบว่าความสามารถในการรักษาโรคของรานั้นเป็นผลมาจากฤทธิ์ต้านแบคทีเรียของราเหล่านั้น ในวิทยานิพนธ์ฉบับนี้ ดูเชสได้ให้เสนอไว้ว่าแบคทีเรียและรานั้นมีการต่อสู้เพื่อความอยู่รอดกันอยู่ตลอดเวลา โดยดูเชสพบว่า แบคทีเรีย E. coli นั้นสามารถถูกกำจัดได้โดยราสายพันธุ์ Penicillium glaucum เมื่อทำการเพาะเลี้ยงจุลชีพทั้งสองในจานเพาะเลี้ยงเดียวกัน นอกจากนี้เขายังพบว่า เมื่อทำการให้เชื้อแบคทีเรียสกุลบาซิลลัสที่เป็นสาเหตุของไข้ไทฟอยด์ พร้อมกับรา Penicillium glaucum แก่สัตว์ทดลองโดยการสูดพ่น พบว่าสัตว์ทดลองนั้น ๆ ไม่ปรากฏอาการและอาการแสดงของไข้ไทฟอยด์ แต่ช่างเป็นที่น่าเสียดายที่ หน่วยบริการทางการทหารที่ดูเชสสังกัดไม่อนุญาตให้เขาทำการศึกษาต่อเนื่องเพิ่มเติมในประเด็นดังกล่าวหลังจากที่เขาจบการศึกษา ภายหลังดูเชสได้เสียชีวิตจากวัณโรค ซึ่งต่อมาก็เป็นอีกโรคหนึ่งที่สามารถรักษาให้หายขาดได้โดยยาปฏิชีวนะ

ต่อมาในปี ค.ศ. 1928, เซอร์ อเล็กซานเดอร์ เฟลมมิง ได้ค้นพบเพนิซิลลิน ซึ่งเป็นสารที่ถูกสร้างขึ้นมาโดยราเพื่อฆ่าหรือหยุดการเจริญเติบโตของแบคทีเรียบางชนิด เฟลมมิงทำงานเพื่อช่วยเหลือทหารที่บาดเจ็บจากสงครามและมีการติดเชื้อแบคทีเรียของแผล ในการเพาะเชื้อแบคทีเรียก่อโรคเขาได้ค้นพบโดยบังเอิญว่าถาดเพาะเชื้อแบคทีเรียก่อโรคในบริเวณที่มีการปนเปื้อนรานั้นไม่มีการเจริญของแบคทีเรียดังกล่าว ซึ่งต่อมาทราบภายหลังว่ารานั้นคือสายพันธุ์ Penicillium chrysogenum เฟลมมิงได้ตั้งสมมติฐานว่าราดังกล่าวอาจหลั่งสารบางอย่างที่มีฤทธิ์ในการต้านแบคทีเรีย เขาได้นำถาดเพาะเชื้อชิ้นนั้นไปเพาะเลี้ยงต่อ แล้วพบว่าเชื้อรานั้นได้ฆ่าแบคทีเรียที่ก่อให้เกิดโรคหลายชนิด และเขาได้ตั้งชื่อสารนั้นว่า เพนิซิลลิน เมื่อวันที่ 7 มีนาคม ค.ศ. 1929 เฟลมมิงเชื่อว่าคุณสมบัติในการต้านแบคทีเรียของสารนี้นั้นอาจเป็นประโยชน์ต่อการรักษาโรคติดเชื้อต่าง ๆ เขาจึงได้เริ่มศึกษาถึงคุณสมบัติทางชีววิทยาของเพนิซิลลินและพยายามที่จะใช้สารสกัดอย่างหยาบ (crude preparation) ที่ได้จากการศึกษาเพื่อรักษาโรคที่เกิดจากการติดเชื้อแบคทีเรียบางชนิด แต่อย่างไรก็ตาม เขาไม่สามารถพัฒนาสารนี้เพิ่มเติมต่อไปได้เนื่องจากไม่มีความช่วยเหลือนักเคมีที่มีความรู้และประสบการณ์
เอินซต์ เชน (Ernst Chain), ฮาเวิร์ด ฟลอเรย์ (Howard Florey) และเอ็ดเวิร์ด อับราฮัม (Edward Abraham) เป็นนักวิทยาศาสตร์กลุ่มแรกที่ประสบความสำเร็จในการสกัดเพนิซิลลินบริสุทธิ์จากราได้ในปี ค.ศ. 1942 โดยยาที่สกัดได้นั้นคือ เบนซิลเพนิซิลลิน (G) แต่ยาดังกล่าวไม่ได้ถูกนำมาใช้ในการรักษาโรคในวงกว้าง โดยจำกัดการใช้อยู่เพียงแต่ภายในกองทัพเท่านั้น แต่หลังจาก ค.ศ. 1945 เป็นต้นมา นอร์มัน ฮีธลีย์ (Norman Heatley) ได้พัฒนาเทคนิคการสกัดแบบย้อนกลับ (back extraction technique) เพื่อให้สกัดเพนิซิลลินในปริมาณมากได้อย่างมีประสิทธิภาพ โดยผู้ที่สามารถถอดแบบโครงสร้างของเพนิซิลลินได้เป็นคนแรกนั้น คือ เอ็ดเวิร์ด อับราฮัม โดยสามารถระบุโครงสร้างที่แน่ชัดดังกล่าวได้ราวปี ค.ศ. 1942 ซึ่งสอดคล้องกับการอธิบายถึงโครงสร้างดังกล่าวในบทความตีพิมพ์ของโดโรธี ฮอดจ์กิน – นักชีวเคมีชาวบริติช เมื่อปี ค.ศ. 1945 โดยเพนิซิลลินสกัดบริสุทธิ์นี้สามารถออกฤทธิ์ต้านแบคทีเรียหลากหลายสายพันธุ์ได้อย่างมีประสิทธิภาพ และก่อให้เกิดพิษต่อมนุษย์ต่ำ นอกจากนี้ ฤทธิ์ของยาดังกล่าวยังไม่ถูกรบกวนโดยส่วนประกอบทางชีวภาพต่าง ๆ ในร่างกาย เช่น หนอง เป็นต้น ซึ่งต่างจากยาสังเคราะห์อย่างซัลโฟนาไมด์ การค้นพบยาปฏิชีวนะที่มีประสิทธิภาพสูงนี้ได้กลายเป็นการเปิดประวัติศาสตร์หน้าใหม่แห่งการแพทย์ โดยการค้นพบและพัฒนาเพนิซิลลินขึ้นมาได้จุดกระแสความสนใจใหม่ให้แก่นักวิจัยในการค้นคว้าหาสารประกอบที่มีฤทธิ์ในการต้านแบคทีเรียใหม่ ๆ ที่มีประสิทธิภาพและความปลอดภัยในระดับเดียวกันกับเพนิซิลลินอีกมากมาย โดยความสำเร็จในการคิดค้นพัฒนาเพนิซิลลินในครั้งนี้ ถึงแม้เฟลมมิงจะค้นพบยาดังกล่าวโดยบังเอิญและไม่สามารถพัฒนายาดังกล่าวได้ด้วยตนเอง ทำให้เขาได้รับรางวัลโนเบลในปี ค.ศ. 1945 ร่วมกับเอินซต์ เชน และฮาเวิร์ด ฟลอเรย์ ในฐานะผู้ค้นพบ และพัฒนาเพนิซิลลินเพื่อใช้ในการรักษาโรคติดเชื้อแบคทีเรียต่าง ๆ ได้สำเร็จ
ฟลอเรย์ได้ยกความดีความชอบให้แก่เรเน ดูบูส์ (Rene Dubos) ที่ได้บุกเบิกคิดค้นวิธีการในการค้นหาสารประกอบที่มีฤทธิ์ต้านแบคทีเรียไว้อย่างดีและเป็นระบบ จนทำให้ดูบูส์ค้นพบกรามิซิดิน และทำให้งานวิจัยเกี่ยวกับเพนิซิลลินของฟลอเรย์เกิดขึ้นมาได้ โดยในปี ค.ศ. 1939 ซึ่งเป็นช่วงเวลาที่ใกล้เกิดสงครามโลกครั้งที่ 2 ดูบูส์ได้ค้นพบสารที่มีฤทธิ์ต้านแบคทีเรียชนิดแรกที่ได้จากธรรมชาติ คือ ไทโรธริซิน ซึ่งเป็นสารที่เป็นส่วนผสมของกรามิซิดิน ร้อยละ 20 และไทโรซิดีน ร้อยละ 80 โดยสกัดสารดังกล่าวได้จากแบคทีเรีย Brevibacillus brevis โดยสารดังกล่าวถือเป็นยาปฏิชีวนะชนิดแรกที่ถูกผลิตออกมาในเชิงการค้า และมีประสิทธิดีเป็นอย่างมากในการรักษาแผลและแผลเปื่อย (ulcer) ในช่วงสงครามโลกครั้งที่ 2 อย่างไรก็ตาม กรามิซิดินไม่สามารถบริหารยาโดยการให้ทางระบบได้ เนื่องจากยาดังกล่าวก่อให้เกิดพิษแก่ร่างกาย เช่นเดียวกันกับไทโรซิดีนที่มีความเป็นพิษเป็นอย่างมากเมื่อเทียบกับกรามิซิดิน ทั้งนี้ องค์ความรู้จากการศึกษาวิจัยต่าง ๆ ที่เกิดขึ้นในช่วงสงครามโลกครั้งที่ 2 นี้ไม่ได้ถูกแบ่งปันกันระหว่างฝ่ายสัมพันธมิตรกับฝ่ายอักษะ ประกอบกับการเข้าถึงข้อมูลได้อย่างจำกัดในช่วงสงครามเย็น ทำให้การต่อยอดหรือพัฒนางานวิจัยต่าง ๆ ในช่วงนั้นมีความก้าวหน้าช้ากว่าที่ควร
การสังเคราะห์ยาปฏิชีวนะจากสีย้อม
ยาปฏิชีวนะสังเคราะห์เป็นวิทยาศาตร์ที่พัฒนาขึ้นแรกเริ่มในเยอรมนีในปีทศวรรษที่ 1880 โดยเพาล์ เอร์ลิช – แพทย์และนักวิทยาศาสตร์ชาวเยอรมันเอร์ลิชพบว่าสีย้อมบางชนิดสามารถทำให้เซลล์สัตว์, มนุษย์ หรือแบคทีเรียติดสีได้ ขณะที่เซลล์สิงมีชีวิตอื่นไม่ติดสีดังกล่าว จากนั้นเขาจึงมีความคิดว่ามีความเป็นไปได้ที่จะใช้สารเคมีบางอย่างที่จำเพาะต่อเซลล์หนึ่ง ๆ มาเป็นยาที่ใช้ฆ่าแบคทีเรียก่อโรคได้โดยไม่ก่อให้เกิดอันตรายแก่มนุษย์ หลังจากนั้นเขาได้ทำการศึกษาสีย้อมที่มีฤทธิ์ต้านจุลชีพหลายร้อยชนิด จนในที่สุด เขาก็ได้พบสารที่มีฤทธิ์ต้านแบคทีเรียที่มีชื่อว่า ซาลวาซาน ในปี ค.ศ. 1907 ซึ่งปัจจุบันรู้จักกันในชื่อ อาร์สเฟนามิน

ยุคของการรักษาด้วยยาปฏิชีวนะนั้นเริ่มต้นขึ้นเมื่อมีการค้นพบยาปฏิชีวนะสังเคราะห์ที่เป็นอนุพันธ์ของสารหนูโดยอัลเฟรด เบอร์ธม (Alfred Bertheim) และเอร์ลิช เมื่อปี ค.ศ. 1907เอร์ลิชและเบอร์ธมได้ศึกษาทดลองรักษาโรคทริปาโนโซมิเอซิสในหนูไมซ์ และการติดเชื้อแบคทีเรียสกุลสไปโรคีทในกระต่ายด้วยสารเคมีจากสีย้อมหลายชนิด การทดลองในช่วงแรกนั้นประสบความล้มเหลวเนื่องจากสีย้อมเหล่านั้นก่อให้เกิดพิษต่อสัตว์ทดลองมากเกินไป ต่อมาเพาล์ เอร์ลิชได้ทำการศึกษาเพื่อค้นหายาปฏิชีวนะในการรักษาซิฟิลิสตามคำร้องขอของกองทัพในขณะนั้น โดยทำการศึกษาร่วมกับซาฮาชิโร ฮาตะ–นักจุลชีววิทยาชาวญี่ปุ่น จนค้นพบสารที่มีคุณสมบัติตามต้องการจากบรรดาสารเคมีที่ทำการศึกษาทั้งหมด 606 ชนิด ใน ค.ศ. 1910 เอร์ลิช และฮาตะได้เผยแพร่การค้นพบที่สำคัญครั้งนี้สู่สาธารณะ ณ งานการประชุมอายุรศาสตร์ที่เมืองวีสบาเดิน โดยทั้งสองได้ตั้งชื่อยาดังกล่าวว่า 606 จากนั้นบริษัทฮุชต์ (Hoechst) ได้เริ่มทำการผลิตยาดังกล่าวออกสู่ตลาดยาในช่วงปลายทศวรรษที่ 1910 ภายใต้ชื่อการค้า Salvarsan ในปัจจุบันยานี้เป็นที่รู้จักกันในชื่อ อาร์สเฟนามิน โดยถูกนำมาใช้เป็นยารักษาซิฟิลิสในช่วงต้นคริสต์ศตวรรษที่ 20 จากการค้นพบอาร์สเฟนามินนี้ ทำให้เอร์ลิชได้รับรางวัลโนเบลสาขาสรีรวิทยาและการแพทย์ในปี ค.ศ. 1908 จากการศึกษาค้นคว้าด้านระบบภูมิคุ้มกัน ส่วนซาฮาชิโร ฮาตะได้รับการเสนอชื่อให้เข้ารับรางวัลโนเบลสาขาเคมีในปี ค.ศ. 1911 และสาขาสรีรวิทยาหรือการแพทย์ในปี ค.ศ. 1912 และ 1913
ยาซัลโฟนาไมด์ชนิดแรกของกลุ่มยานี้อย่าง พรอนโตซิล ถือเป็นยาปฏิชีวนะสังเคราะห์ชนิดแรกที่อยู่ในรูปแบบที่พร้อมออกฤทธิ์ได้ โดยยาดังกล่าวถูกพัฒนาขึ้นในช่วงปี ค.ศ. 1932–1933 โดยทีมนักวิจัยที่นำทีมโดย แกร์ฮาร์ด โดมักค์ ณ ห้องปฏิบัติการของบริษัทไบเออร์ ซึ่งเป็นบริษัทในเครือของกลุ่มบริษัทไอ.จี.ฟาร์เบินในประเทศเยอรมนี การค้นพบนี้ทำให้โดมักค์ได้รับรางวัลโนเบลสาขาสรีรวิทยาหรือการแพทย์ในปี ค.ศ. 1939 ส่วนซัลฟานิลาไมด์ซึ่งเป็นรูปแบบที่ออกฤทธิ์ของพรอนโตซิลนั้นไม่ได้รับอนุญาตให้จดสิทธิบัตร เนื่องจากสารดังกล่าวนั้นถูกใช้ในอุตสาหกรรมสีย้อมก่อนหน้ามาเป็นเวลาหลายปีแล้วพรอนโตซิลเป็นยาปฏิชีวนะที่มีขอบเขตการออกฤทธิ์ค่อนข้างกว้าง โดยมีฤทธิ์ต้านแบคทีเรียแกรมบวกทรงกลม (cocci) ได้ดี แต่ไม่มีฤทธิ์ต่อวงศ์เอนเทอร์โรแบคทีเรียซีอี การค้นพบพรอนโตซิลนี้เป็นการเปิดศักราชใหม่ของการแพทย์ที่ส่งผลเกิดการตื่นตัวในการคิดค้นพัฒนายาปฏิชีวนะอื่นตามมาเป็นอย่างมาก
การใช้ประโยชน์ทางการแพทย์
ยาปฏิชีวนะเป็นยาที่ถูกใช้ในการรักษาและป้องกันการติดเชื้อแบคทีเรีย และในบางครั้งถูกใช้เป็นยาต้านโพรโทซัว (เมโทรนิดาโซล สำหรับรักษาโรคที่เกิดจากการติดเชื้อโพรโตซัวบางสายพันธุ์ และในบางครั้งก็อาจถูกนำมาใช้เป็นยาต้านปรสิตได้เช่นกัน เมื่อพบว่ามีการติดเชื้อแบคทีเรียหรือมีอาการที่อาจบ่งบอกได้ว่าเป็นการติดเชื้อแบคทีเรีย แต่ยังไม่สามารถจำแนกสายพันธุ์ของเชื้อก่อโรคได้ จะมีการให้การรักษาด้วยยาปฏิชีวนะที่เรียกว่า การให้ยาปฏิชีวนะแบบครอบคลุมเชื้ออย่างกว้าง (empiric therapy) เพื่อให้ครอบคลุมเชื้อที่อาจเป็นสาเหตุทั้งหมด อย่างไรก็ตาม การให้ยาปฏิชีวนะที่ออกฤทธิ์กว้าง (broad-spectrum antibiotic) จะขึ้นอยู่อาการและอาการแสดงของผู้ป่วยและผลการจรวจทางห้องปฏิบัติการในแต่ละวัน ซึ่งอาจต้องใช้เวลาหลายวันในการระบุเชื้อสาเหตุที่แน่ชัดได้
เมื่อทราบถึงสายพันธุ์ของเชื้อก่อโรคดังข้างต้นแล้ว แบบแผนการรักษาด้วยยาปฏิชีวนะจะถูกปรับเปลี่ยนให้จำเพาะเจาะจงกับเชื้อสาเหตุนั้น ๆ มากขึ้น โดยทั่วไปมักเลือกใช้ยาปฏิชีวนะที่มีขอบเขตการออกฤทธิ์ครอบคลุมเชื้อที่แคบลง (narrow-spectrum antibiotic) ทั้งนี้ การปรับเปลี่ยนแบบแผนการรักษานี้จะขึ้นอยู่กับข้อบ่งใช้ ราคา ประสิทธิภาพ ความปลอดภัย และความสะดวกในการใช้ยานั้น การระบุชนิดของเชื้อก่อโรคที่จำเพาะถือเป็นจุดสำคัญในการรักษา เนื่องจากจะช่วยลดค่าใช้จ่าย รวมไปถึงความเสี่ยงที่อาจเกิดพิษหรืออาการไม่พึงประสงค์ จากการที่ต้องได้รับการรักษายาปฏิชีวนะที่ออกฤทธิ์กว้างหรือหลายชนิดร่วมกัน อีกทั้งยังช่วยลดความเป็นไปได้ที่จะเกิดภาวะเสี่ยงจากการดื้อยาของเชื้อแบคทีเรียได้ด้วย ในอีกกรณีหนึ่ง การมีการใช้ยาปฏิชีวนะในผู้ป่วยที่มีภาวะไส้ติ่งอักเสบเฉียบพลัน เป็นการรักษาอีกหนึ่งทางเลือกโดยไม่ต้องทำการผ่าตัด
นอกจากนี้แล้ว ยังมีการใช้ยาปฏิชีวนะเพื่อเป็นการป้องกัน (prophylactic) เฉพาะในผู้ที่มีความเสี่ยงต่อการติดเชื้อแบคทีเรียสูง เช่น ผู้ที่มีภูมิคุ้มกันบกพร่อง (โดยเฉพาะผู้ป่วยเอดส์ เพื่อป้องกันโรคปอดบวม), ผู้ที่กำลังอยู่ระหว่างการใช้ยากดภูมิคุ้มกัน, ผู้ป่วยมะเร็ง และผู้ป่วยที่ต้องได้รับการผ่าตัด อาจการใช้ยาปฏิชีวนะก่อนและหลังการผ่าตัดเพื่อช่วยป้องกันการติดเชื้อแบคทีเรียบริเวณแผล และมีการใช้ในทางทันตกรรมเพื่อเป็นการป้องกันการติดเชื้อแบคทีเรียในกระแสเลือดและการเกิดภาวะเยื่อบุหัวใจอักเสบติดเชื้อ รวมไปถึงการใช้ยาปฏิชีวนะในการป้องกันการติดเชื้อแบคทีเรียในผู้ป่วยที่มีนิวโตรฟิลในเลือดต่ำ โดยเฉพาะอย่างยิ่ง ในผู้ป่วยมะเร็ง
โดยยาปฏิชีวนะต่างชนิดหรือต่างกลุ่มกันจะมีข้อบ่งใช้สำหรับการติดเชื้อแบคทีเรียที่แตกต่างกันออกไป ดังแสดงในตารางต่อไปนี้
การบริหารยา
การบริหารยาปฏิชีวนะนั้นสามารถกระทำได้หลายช่องทาง โดยปกติแล้วมักใช้การบริหารยาโดยการรับประทานทางปาก แต่ในกรณีที่ผู้ป่วยมีอาการรุนแรง โดยเฉพาะอย่ายิ่ง ในผู้ป่วยที่มีการติดเชื้อในกระแสเลือดอย่างรุนแรง จะบริหารยาให้แก่ผู้ป่วยด้วยวิธีการฉีดเข้าหลอดเลือดดำ หรือการฉีดอื่น ในกรณีที่ตำแหน่งที่เกิดการติดเชื้ออยู่ในบริเวณที่ยาปฏิชีวนะสามารถแพร่กระจายเข้าไปได้โดยง่าย อาจบริหารยาปฏิชีวนะนั้น ๆ ได้ด้วยการใช้ในรูปแบบยาใช้ภายนอก อาทิ การใช้ยาหยอดตาหยอดลงเยื่อบุตาในกรณีเยื่อบุตาอักเสบ หรือการใช้ยาหยอดหู ในกรณีติดเชื้อแบคทีเรียในหูหรือหูชั้นนอกอักเสบเฉียบพลัน (acute otitis externa) ยาใช้ภายนอกในรูปแบบยาทาเป็นอีกทางเลือกหนึ่งสำหรับผู้ที่มีการติดเชื้อบริเวณผิวหนังที่ไม่รุนแรง เช่น สิวอักเสบจากการติดเชื้อแบคทีเรีย (acne vulgaris) และเซลล์เนื้อเยื่ออักเสบ (Cellulitis) โดยประโยชน์จากการใช้ยาปฏิชีวนะในรูปแบบยาใช้ภายนอก ได้แก่ บริเวณที่เกิดการติดเชื้อจะมีความเข้มข้นของยาสูงและมีความสม่ำเสมอ, ลดความเสี่ยงที่อาจเกิดพิษหรืออาการไม่ประสงค์บางอย่างจากการใช้ยา, และปริมาณยาที่ต้องใช้ในการรักษาลดลง นอกจากนี้ยังลดปริมาณการใช้ยาปฏิชีวนะในทางที่ผิดได้อีกด้วย นอกจากนี้ การทายาปฏิชีวนะชนิดทาในกรณีแผลผ่าตัดนั้นก็สามารถลดความเสี่ยงในการเกิดการติดเชื้อในแผลผ่าตัดได้ อย่างไรก็ตาม ยังมีบางประเด็นที่กังวลเกี่ยวกับการใช้ยาปฏิชีวนะชนิดใช้ภายนอก เนื่องจากอาจมีการดูดซึมยาเข้าสู่กระแสเลือดได้ในบางกรณี, ปริมาณยาที่ใช้ในแต่ละครั้งนั้นยากที่จะกำหนดให้แม่นยำได้ และอาจทำให้เกิดภาวะภูมิไวเกิน หรือผื่นแพ้สัมผัสได้
อาการไม่พึงประสงค์
ยาปฏิชีวนะนั้นจำเป็นต้องมีการศึกษาทดลองเพื่อค้นหาอาการไม่พึงประสงค์ต่าง ๆ ของยาที่อาจเกิดขึ้นได้ก่อนจะมีการอนุมัติให้ใช้เพื่อการบำบัดรักษาโรคในมนุษย์ และยาที่ได้รับอนุมัตินั้นต้องมีความปลอดภัยและผู้ป่วยสามารถยอมรับหรือทนต่ออาการข้างเคียงที่อาจเกิดขึ้นได้ อย่างไรก็ตาม ยาปฏิชีวนะบางชนิดนั้นมีความสัมพันธ์กับการเกิดอาการไม่พึงประสงค์หลายอย่าง ตั้งแต่รุนแรงเล็กน้อยไปจนถึงรุนแรงมาก ขึ้นอยู่กับชนิดของยาปฏิชีวนะที่ถูกใช้, จุลชีพเป้าหมาย, และปัจจัยอื่นที่เป็นปัจเจกอาการไม่พึงประสงค์จากยานั้นอาจเป็นผลมาจากมาจากคุณสมบัติทางเภสัชวิทยาหรือพิษวิทยาของยานั้นหรือเกิดจากการเหนี่ยวนำให้เกิดภาวะภูมิไวเกิน หรือปฏิกิริยาการแพ้ยา โดยอาการไม่พึงประสงค์ที่เกิดขึ้นอาจมีตั้งแต่ ไข้ หนาวสั่น คลื่นไส้ ไปจนถึงอาการที่รุนแรงอย่างปฏิกิริยาการแพ้ยาได้ เช่น ผื่นแพ้แสงแดด (photodermatitis) และปฏิกิริยาภูมิแพ้เฉียบพลันรุนแรง (Anaphylaxis) ทั้งนี้ ข้อมูลด้านความปลอดภัยของยาใหม่นั้น โดยปกติแล้วมักมีข้อมูลไม่ครอบคลุมอาการไม่พึงประสงค์ที่อาจเกิดขึ้นได้เทียบเท่ากับยาเก่าที่มีการใช้ในมนุษย์มาเป็นเวลานาน
อาการไม่พึงประสงค์จากยาปฏิชีวนะที่เกิดขึ้นได้ทั่วไปในผู้ที่ได้รับการรักษาด้วยยาปฏิชีวนะอย่าง อาการท้องเสียนั้นเป็นผลมาจากการรบกวนสมดุลเชื้อจุลินทรีย์ประจำถิ่นในลำไส้ (intestinal flora) ทำให้เกิดการเจริญเติบโตของเชื้อแบคทีเรียก่อโรคอื่น ๆ เช่น Clostridium difficile นอกจากนี้ ยาปฏิชีวนะยังส่งผลต่อสมดุลเชื้อจุลินทรีย์ประจำถิ่นในช่องคลอด (vaginal flora) ได้ด้วย ทำให้เกิดการเพิ่มจำนวนขึ้นของยีสต์สกุลแคนดิดาในช่องคลอดและบริเวณปากช่องคลอดได้ ทั้งนี้ อาการไม่พึงประสงค์จากยาปฏิชีวนะอาจเกิดขึ้นได้จากการเกิดอันตรกิริยาระหว่างยา (drug interaction) ระหว่างยาปฏิชีวนะกับยาอื่นได้ เช่น ความเสี่ยงที่อาจเกิดความเสียหายต่อเอ็นกล้ามเนื้อ (tendon) จากการใช้ยาปฏิชีวนะกลุ่มควิโนโลน (quinolone antibiotic) ร่วมกับคอร์ติโคสเตอรอยด์ที่ให้ผ่านทางระบบ
สหสัมพันธ์กับโรคอ้วน
การสัมผัสกับยาปฏิชีวนะในช่วงต้นของชีวิตมีความสัมพันธ์กับการเพิ่มขึ้นของมวลกายในมนุษย์และหนูทดลอง ทั้งนี้ เนื่องมาจากในช่วงตอนต้นของชีวิตนั้นเป็นช่วงที่มีการสร้างสมจุลินทรีย์ประจำถิ่นในลำไส้ และการพัฒนาระบบเมแทบอลิซึมของร่างกาย ในหนูทดลองที่สัมผัสกับยาปฏิชีวนะในระดับที่ต่ำกว่าที่ใช้ในการรักษาโรค (subtherapeutic antibiotic treatment; STAT) ชนิดใดชนืดหนึ่ง ได้แก่ เพนิซิลลิน, แวนโคมัยซิน, หรือ คลอร์เตตราไซคลีน นั้นจะเกิดการรบกวนการสร้างสมจุลินทรีย์ประจำถิ่นในลำไส้ รวมไปถึงความสามารถในการเผาผลาญสารอาหารของร่างกาย (metabolism) มีการศึกษาที่พบว่าหนูไมซ์ (mice) ที่ได้รับยาเพนิซิลลินในขนาดต่ำ (1 ไมโครกรัม/น้ำหนักตัว 1 กรัม) ตั้งแต่แรกเกิดจนถึงช่วงหย่านม มีการเพิ่มขึ้นของมวลร่างกายและมวลไขมัน, มีการเจริญเติบโตที่เร็วมากขึ้น, และมีการเพิ่มการแสดงออกของยีนของตับที่เหนี่ยวนำให้เกิดกระบวนการสร้างเซลล์ไขมัน ในอัตราที่มากกว่าหนูตัวอื่นในกลุ่มควบคุมที่ไม่ได้รับยาปฏิชีวนะ นอกจากนี้ การได้รับเพนิซิลลินร่วมกับอาหารที่มีปริมาณไขมันสูงนั้นมีผลเพิ่มระดับอินซูลินขณะที่ท้องว่างในหนูไมซ์ อย่างไรก็ตาม ยังไม่เป็นทราบแน่ชัดว่า โดยแท้จริงแล้วยาปฏิชีวนะเป็นสาเหตุหนึ่งที่ทำให้เกิดโรคอ้วนในมนุษย์ได้หรือไม่ การศุกษาบางการศึกษาพบการมีสหสัมพันธ์ระหว่างการได้รับยาปฏิชีวนะตั้งแต่ในวัยทารก (อายุ <6 เดือน) กับการเพิ่มขึ้นของมวลกาย (ที่อายุ 10 และ 20 เดือน) อีกการศึกษาหนึ่งพบว่า ชนิดของยาปฏิชีวนะที่ได้รับนั้นมีความสัมพันธ์กับการเกิดโรคอ้วน โดยผู้ที่ได้รับยากลุ่มแมโครไลด์ จะมีความเสี่ยงต่อการเกิดภาวะน้ำหนักเกินสูงกว่าผู้ที่ได้รับยาเพนิซิลลินหรือเซฟาโลสปอรินอย่างมีนัยสำคัญ ดังนั้น จึงอาจสรุปได้ว่าการได้รับยาปฏิชีวนะในช่วงวัยทารกนั้นมีความสัมพันธ์กับการเกิดโรคอ้วนในมนุษย์ แต่ความสัมพันธ์เชิงเหตุผลในประเด็นดังกล่าวนั้นยังไม่เป็นที่ทราบแน่ชัด ทั้งนี้ ถึงแม้ว่าจะมีความสัมพันธ์ระหว่างการเกิดโรคอ้วนกับการได้รับยาปฏิชีวนะก็ตาม การใช้ยาปฏิชีวนะในทารกก็ควรที่จะชั่งน้ำหนักถึงความเสี่ยงที่อาจเกิดขึ้นกับประโยชน์ทางคลินิกที่จะได้รับอยู่เฉกเช่นเดิมเสมอ
อันตรกิริยา
ยาเม็ดคุมกำเนิด
การศึกษาทางคลินิกที่มีคุณภาพสูงที่ศึกษาเกี่ยวกับความสัมพันธ์ระหว่างผลของการยาปฏิชีวนะต่อประสิทธิภาพในการคุมกำเนิดของยาเม็ดคุมกำเนิดชนิดรับประทานนั้นยังมีไม่มากนัก การศึกษาหลายการศึกษาให้ผลลัพธ์ที่บ่งชี้ว่ายาปฏิชีวนะไม่มีผลรบกวนการออกฤทธิ์คุมกำเนิดของยาเม็ดคุมกำเนิดชนิดรับประทานแต่อย่างใด นอกจากนี้ การศึกษาเหล่านั้นยังลงความเห็นไว้ว่า อัตราการคุมกำเนิดล้มเหลวในผู้ที่ใช้วิธีการคุมกำเนิดโดยการรับประทานยาเม็ดคุมกำเนิดนั้นอยู่ในสัดส่วนที่ต่ำมาก (ประมาณร้อยละ 1) โดยสภาวะที่อาจเพิ่มความเสี่ยงต่อการคุมกำเนิดด้วยาเม็ดคุมกำเนิดแล้วล้มเหลวนั้นได้แก่ ความร่วมมือในการใช้ยา (ลืมรับประทานยา), อาเจียน หรือท้องเสีย ความผิดปกติของระบบทางเดินอาหาร หรือความแตกต่างของปัจจัยอื่นระดับบุคคลที่ส่งผลต่อการดูดซึมนั้นจะส่งผลต่อระดับความเข้มข้นของฮอร์โมนเอทินิลเอสทราไดออลในกระแสเลือดได้ นอกจากนี้ ผู้หญิงที่มีประจำมาไม่ปกติเป็นประจำอาจเพิ่มความเสี่ยงต่อการเกิดความล้มเหลวในการคุมกำเนิดด้วยาคุมกำเนิดชนิดรับประทานได้ และควรได้รับคำแนะนำให้ใช้วิธีการคุมกำเนิดอื่นร่วมด้วยเพิ่มเติมในช่วงเวลาที่จำเป็นต้องใช้ยาปฏิชีวนะเพื่อรักษาโรคและในช่วง 1 สัปดาห์หลังหยุดใช้ยาปฏิชีวนะ หากพบว่าผู้ป่วยมีความเสี่ยงอื่นใดที่ส่งผลลดประสิทธิภาพของยาเม็ดคุมกำเนิดชนิดรับประทาน แนะนำให้ใช้วิธีการคุมกำเนิดอย่างอื่นร่วมด้วย เพื่อลดความเสี่ยงในการตั้งครรภ์
ในกรณที่พบว่ายาปฏิชีวนะมีผลต่อประสิทธิภาพในการคุมกำเนิดของยาเม็ดคุมกำเนิด เช่น ในกรณีของไรแฟมพิซิน ซึ่งเป็นยาปฏิชีวนะนั้นออกฤทธิ์กว้างครอบคลุมเชื้อแบคทีเรียหลายชนิด โดยยานี้จะส่งผลต่อประเด็นดังกล่าวได้เนื่องจากยาจะทำให้เอนไซม์ของตับทำงานมากขึ้น ทำให้มีการกำจัดฮอร์โมนเอทินิลเอสทราไดออล ซึ่งเป็นฮอร์โมนที่ใช้ในการคุมกำเนิด ออกจากร่างกายในอัตราที่มากขึ้น ซึ่งจะส่งผลเพิ่มความเสี่ยงต่อการตั้งครรภ์ได้มากกว่าปกติ นอกจากนี้ ยาปฏิชีวนะดังกล่าวจะทำลายจุลินทรีย์ประจำถิ่นในทางเดินอาหาร ซึ่งทำหน้าที่ในการเปลี่ยนเมตาบอไลต์ของเอทินิลเอสทราไดออลให้อยู่ในรูปที่ถูกดูดซึมกลับเข้าไปในกระแสเลือดได้ใหม่อีกครั้ง การที่จุลินทรีย์ประจำถิ่นในทางเดินอาหารถูกทำลาย จะทำให้การดูดซึมกลับฮอร์โมนคุมกำเนิดลดน้อยลงได้ อย่างไรก็ตาม ในปัจจุบัน ประเด็นที่เกี่ยวเนื่องกับจุลินทรีย์ประจำถิ่นในทางเดินอาหารนี้ยังเป็นที่ถกเถียงกันอยู่ในทางวิชาการและยังไม่สามารถหาข้อสรุปที่แน่ชัดได้ ดังนั้น บุคลากรทางการแพทย์จึงควรให้คำแนะนำแก่ผู้อยู่ระหว่างการคุมกำเนิดด้วยาเม็ดคุมกำเนิดชนิดรับประทานที่จำเป็นต้องที่ได้รับการรักษาด้วยยาปฏิชีวนะที่อาจส่งผลต่อประสิทธิภาพในการคุมกำเนิดให้ใช้วิธีการคุมกำเนิดอื่นร่วมด้วย เพื่อลดความเสี่ยงในการตั้งครรภ์ไม่พึงประสงค์ แต่ในท้ายที่สุดแล้ว ผลของยาปฏิชีวนะต่อประสิทธิภาพในการคุมกำเนิดของยาเม็ดคุมกำเนิดชนิดรับประทานนั้นยังจำเป็นต้องอาศัยข้อมูลจากการศึกษาวิจัยทางคลินิกเพิ่มเติมอีกในอนาคต เพื่อหาข้อสรุปและปัจจัยต่าง ๆ ที่มีผลให้แน่ชัดมากขึ้น
เครื่องดื่มแอลกอฮอล์
อันตรกิริยาระหว่างแอลกอฮอล์กับยาปฏิชีวนะนั้นอาจพบเกิดขึ้นได้ในบางกรณี โดยอาจทำให้เกิดอาการไม่พึงประสงค์ในระดับที่เล็กน้อยไปจนถึงระดับที่อันตรายถึงชีวิต หรือในบางครั้งอันตรกิริยานี้อาจส่งผลลดประสิทธิภาพในการรักษาของยาปฏิชีวนะชนิดนั้น ๆ ลงได้การบริโภคเครื่องดื่มแอลกอฮอล์ในปริมาณเพียงเล็กน้อยถึงปานกลางนั้นพบว่าไม่มีผลรบกวนการออกฤทธิ์หรือประสิทธิภาพของยาปฏิชีวนะทั่วไป แต่ยาปฏิชีวนะบางกลุ่มนั้น การบริโภคเครื่องดื่มแอลกอฮอล์ร่วมด้วยแม้เพียงในปริมาณเล็กน้อยก็อาจทำให้เกิดอาการไม่พึงประสงค์จากยาได้ ทั้งนี้ ความรุนแรงของอาการไม่พึงประสงค์ที่เกิดขึ้นและประสิทธิภาพของยาปฏิชีวนะที่เปลี่ยนแปลงไปจากสาเหตุข้างต้นนั้นจะขึ้นอยู่กับชนิดและรูปแบบของยาปฏิชีวนะที่ได้รับอยู่ในขณะนั้นด้วย
ยาปฏิชีวนะบางชนิดอย่างเมโทรนิดาโซล, ทินิดาโซล, เซฟาแมนโดล, ลาตามอกเซฟ, เซโฟเพอราโซน, เซฟมีนอกซิม, และฟูราโซลิโดน นั้นสามารถทำให้เกิดกลุ่มอาการคล้ายปฏิกิริยาจากยาไดซัลฟิแรม (Disulfiram-like Reaction) ได้หากมีการบริโภคเครื่องดื่มแอลกอฮอล์ร่วมด้วยระหว่างที่ได้รับยาเหล่านี้ โดยแอลกอฮอล์จะถูกเปลี่ยนแปลงในร่างกายได้น้อยลง เนื่องจากยามีผลยับยั้งการทำงานของเอนไซม์ acetaldehyde dehydrogenase ซึ่งทำหน้าที่เปลี่ยนแปลงแอซีทาลดีไฮด์ซึ่งเป็นสารพิษที่ได้จากการเปลี่ยนแปลงแอลกอฮอล์ของร่างกายให้เป็นกรดแอซิติก ซึ่งเป็นรูปสารที่ไม่ก่อให้เกิดอันตรายแก่ร่างกาย และกกรดแอซิติกนี้จะถูกกำจัดออกจากร่างกายต่อไปทางปัสสาวะ โดยกลุ่มอาการคล้ายปฏิกิริยาจากยาไดซัลฟิแรมนี้จะมีอาการสำคัญ คือ คลื่นไส้ อาเจียน หายใจหอบเหนื่อย หน้าแดง ความดันโลหิตเพิ่มขึ้น นอกจากนี้ ดอกซีไซคลีน และอิริโทรมัยซิน ซัคซิเนท อาจมีประสิทธิภาพลดลงได้หากดื่มเครื่องดื่มแอลกอฮอล์ในระหว่างที่ได้รับการรักษาด้วยยาชนิดนี้ ส่วนผลอื่น ๆ ของแอลกอฮอล์ต่อการออกฤทธิ์ของยาปฏิชีวนะนั้นอาจเป็นผลมาจากการที่แอลกอฮอล์รบกวนการทำงานของเอนไซม์ตับ ซึ่งอาจทำให้ยาปฏิชีวนะบางชนิดถูกกำจัดออกจากร่างกายได้มากขึ้นได้
เภสัชพลศาสตร์
ผลลัพธ์ที่ดีจากการได้รับการรักษาด้วยาปฏิชีวนะนั้นขึ้นอยู่กับหลายปัจจัย ได้แก่ ระบบภูมิคุ้มกันของแต่ละคน, ตำแหน่งที่เกิดการติดเชื้อแบคทีเรีย, และคุณสมบัติทางเภสัชพลศาสตร์และเภสัชจลนศาสตร์ของยาปฏิชีวนะที่ใช้ในการรักษา ฤทธิ์ในการฆ่าเชื้อแบคทีเรียของยาปฏิชีวนะนั้นอาจจะขึ้นอยู่กับระยะการเจริญเติบโตของแบคทีเรียก่อโรค และอัตราการเกิดเมแทบอลิซึมภายในเซลล์ของแบคทีเรีย รวมไปถึงความเร็วในการแบ่งตัวของแบคทีเรียชนิดนั้น ๆ อีกด้วย โดยปัจจัยที่กล่าวมาดังข้างต้นล้วนเป็นผลลัพธ์ที่ได้มาจากการศึกษาทดลองภายในห้องปฏิบัติการและล้วนให้ผลที่สอดคล้องกับการบำบัดรักษาจริงในทางคลินิก ทั้งนี้ เนื่องจากการออกฤทธิ์ในการต้านแบคทีเรียของยาปฏิชีวนะนั้นขึ้นอยู่กับความเข้นข้นของยาปฏิชีวนะชนิดนั้น ๆ การศึกษานอกร่างกายมนุษย์ ซึ่งทดลองภายในห้องปฏิบัติการ (in vitro) ได้มีการจำแนกประสิทธิภาพในการออกฤทธิ์ต้านแบคทีเรียของยาปฏิชีวนะโดยใช้ ความเข้มข้นของยาต่ำสุดที่สามารถยับยั้งการเจริญเติบโตของเชื้อแบคทีเรีย (minimum inhibitory concentration; MIC) และ ความเข้มข้นยาต่ำสุดที่ฆ่าแบคทีเรียได้ร้อยละ 90 (minimum bactericidal concentration; MBC) โดยใช้ค่าดังกล่าว ร่วมกับคุณสมบัติทางเภสัชจลนศาสตร์ของยาปฏิชีวนะชนิดนั้น ๆ และคุณลักษณะอื่นทางเภสัชวิทยาในการทำนายประสิทธิภาพและผลลัพธ์การรักษาของยาปฏิชีวนะชนิดใดชนิดหนึ่งในทางคลินิก
การใช้ยาปฏิชีวนะหลายขนาน
ในการรักษาโรคที่เกิดจากการติดเชื้อแบคทีเรียที่รุนแรงบางชนิด เช่น วัณโรค เป็นต้น การรักษาด้วยยาหลายขนาน (การรักษาด้วยยาปฏิชีวนะอย่างน้อย 2 ชนิดขึ้นไป) จะถูกนำมาพิจารณาใช้เพื่อชะลอหรือป้องกันการดื้อต่อยาปฏิชีวนะของเชื้อสาเหตุ ในกรณีที่เป็นการติดเชื้อแบคทีเรียแบบเฉียบพลัน ยาปฏิชีวนะที่เลือกใช้ในการรักษาด้วยยาหลายขนานนี้จะต้องเป็นยาเสริมฤทธิ์ซึ่งกันและกันจะทำให้มีประสิทธิภาพในการรักษามากกว่าการใช้ยาปฏิชีวนะเพียงชนิดเดียว เช่น ในกรณีการติดเชื้อ Staphylococcus aureus ที่ดื้อต่อเมทิซิลลินนั้น อาจให้การรักษาด้วยกรดฟูซิดิค และไรแฟมพิซินร่วมกัน ในทางตรงกันข้าม ยาปฏิชีวนะบางชนิดนั้นเมื่อถูกนำมาใช้ร่วมกันอาจแสดงคุณสมบัติต้านฤทธิ์ซึ่งกันและกัน และทำให้ผลลัพธ์และประสิทธิภาพในการรักษานั้นต่ำกว่าการใช้ยาปฏิชีวนะชนิดนั้นเพียงชนิดเดียวได้เช่นกัน เช่น คลอแรมเฟนิคอล และเตตราไซคลีน จะต้านฤทธิ์ของยากลุ่มเพนิซิลลิน และอะมิโนไกลโคไซด์ อย่างไรก็ตาม การเลือกใช้ยาปฏิชีวนะในกรณีนั้นมีความหลากหลายมากขึ้นอยู่กับชนิดของเชื้อสาเหตุและตำแหน่งที่เกิดการติดเชื้อแบคทีเรีย แต่โดยปกติแล้ว ยาปฏิชีวนะที่ออกฤทธิ์ต้านการเจริญเติบโตของแบคทีเรีย (bacteriostatic antibiotic) มักออกฤทธิ์ต้านกันกับยาปฏิชีวนะที่ออกฤทธิ์ฆ่าเชื้อแบคทีเรีย (bactericidal antibiotic)
การแบ่งกลุ่มยาปฏิชีวนะ
โดยปกติแล้วการแบ่งกลุ่มยาปฏิชีวนะนั้นจะแบ่งตามกลไกการออกฤทธิ์, โครงสร้างทางเคมี หรือขอบเขตการออกฤทธิ์ โดยมีเป้าหมายการออกฤทธิ์มุ่งไปที่การขัดขวางการทำงานในระดับเซลล์หรือการเจริญเติบโตของแบคทีเรีย ซึ่งเป้าหมายเหล่านั้นอาจเป็นผนังเซลล์ (กลุ่มเพนิซิลลิน และกลุ่มเซฟาโลสปอริน) หรือเยื่อหุ้มเซลล์ (พอลีมิกซิน) หรือรบกวนการทำงานของเอนไซม์ที่จำเป็นของแบคทีเรีย (กลุ่มไรฟามัยซิน, กลุ่มลิปิอาร์มัยซิน, กลุ่มควิโนโลน, และกลุ่มซัลโฟนาไมด์) โดยที่ออกฤทธิ์ที่ตำแหน่งดังข้างต้นนั้นจะมีคุณสมบัติเป็น ยาปฏิชีวนะที่ออกฤทธิ์ฆ่าเชื้อแบคทีเรีย (bactericidal antibiotic) ส่วนยาปฏิชีวนะอื่นที่ออกฤทธิ์ยับยั้งการสังเคราะห์โปรตีนของแบคทีเรีย (กลุ่มแมโครไลด์, กลุ่มลินโคซาไมด์ และเตตราไซคลีน) จะเป็น ยาปฏิชีวนะที่ออกฤทธิ์ยับยั้งการเจริญเติบโตเชื้อแบคทีเรีย (bacteriostatic antibiotic) ยกเว้นกลุ่มอะมิโมไกลโคไซด์ที่ออกฤทธิ์ฆ่าเชื้อแบคทีเรีย นอกเหนือไปจากนี้มักเป็นการแบ่งตามความจำเพาะในการออกฤทะกับเป้าหมาย ยกตัวอย่างเช่น ยาปฏิชีวนะที่มีขอบเขตการออกฤทธิ์แคบ (Narrow-spectrum antibiotics) จะหมายถึงยาปฏิชีวนะที่ออกฤทธิ์จำเพาะต่อแบคทีเรียกลุ่มใดกลุ่มหนึ่ง อาทิ แบคทีเรียแกรมลบ หรือแบคทีเรียแกรมบวก เป็นต้น ในขณะที่ ยาปฏิชีวนะที่มีขอบเขตการออกฤทธิ์กว้าง (Broad-spectrum antibiotics) จะออกฤทธิ์ต่อแบคทีเรียได้หลายกลุ่ม นอกเหนือจากการแบ่งกลุ่มดังข้างต้น ได้มีการคิดค้นพัฒนายาปฏิชีวนะกลุ่มใหม่เพิ่มขึ้นอีกจำนวนหนึ่ง ซึ่งหากย้อนไปในอดีตราว 40 กว่าปีที่แล้วตั้งแต่ที่มีการค้นพบสารประกอบกลุ่มใหม่ที่มีคุณสมบัติในการต้านแบคทีเรีย ก็ไม่ได้มีการค้นพบยาปฏิชีวนะกลุ่มใหม่เพิ่มขึ้นเท่าใดนัก จนกระทั่งในช่วงปลายคริสต์ทศวรรตที่ 2000 และต้นคริสต์ทศวรรตที่ 2010 ได้มีการพัฒนาคิดค้นยาปฏิชีวนะกลุ่มใหม่ขึ้นได้สำเร็จและถูกนำมาใช้ทางคลินิกมากถึง 4 กลุ่ม ได้แก่ กลุ่มไลโปเพปไทด์ (เช่น แดพโตมัยซิน), กลุ่มไกลซิลไซคลีน (เช่น ไทกีไซคลีน), กลุ่มออกซาโซลิไดโอน (เช่น ไลนิโซลิด), และ กลุ่มลิปิอาร์มัยซิน (เช่น ฟิแดกโซมัยซิน)
ทั้งนี้ การแบ่งยาปฏิชีวนะตามกลไกการออกฤทธิ์โดยสังเขปแล้วสามารถแบ่งได้ตามตารางต่อไปนี้:
| ชื่อสามัญทางยา | ชื่อการค้า | ข้อบ่งใช้ | อาการไม่พึงประสงค์ | กลไกการออกฤทธิ์ |
|---|---|---|---|---|
| อะมิโนไกลโคไซด์ | ||||
| อะมิกาซิน | Amikin | การติดเชื้อแบคทีเรียแกรมลบอย่างรุนแรง ได้แก่ Escherichia coli และ Klebsiella โทบรามัยซิน ออกฤทธิ์ต่อ Pseudomonas aeruginosa ได้ดีมาก นีโอมัยซิน สามารถใช้เพื่อป้องกันการติดเชื้อแบคทีเรียในผู้ที่ต้องได้รับการผ่าตัดบริเวณช่องท้องได้ ยากลุ่มนี้มีประสิทธิภาพดีในการรักษาโรคที่เกิดจากการติดเชื้อที่เกิดจากเชื้อแบคทีเรียกลุ่มที่ไม่ใช้ออกซิเจน (ยกเว้นสายพันธุ์ที่เจริญได้ทั้งที่มีและไม่มีออกซิเจน; Facultative anaerobe) เนติลมัยซิน สามารถออกฤทธิ์ต่อเชื้อแบคทีเรียที่ดื้อต่อเจนตามัยซินและโทบรามัยซินได้ดี |
|
ยับยั้งการสังเคราะห์โปรตีน โดยจับกับหน่วยย่อย 30 เอสของไรโบโซมแบคทีเรีย ทำให้การแปรรหัสพันธุกรรมผิดพลาด และได้โปรตีนที่ไม่สามารถทำงานได้ |
| เจนตามัยซิน | Garamicina | |||
| กานามัยซิน | Kantrex | |||
| นีโอมัยซิน | Neosporin | |||
| เนติลมัยซิน | Netromicina | |||
| สเตรปโตมัยซิน | ||||
| โทบรามัยซิน | Nebcin | |||
| พาโรโมมัยซิน | Humatin | |||
| เอนซามัยซิน | ||||
| เกลดานามัยซิน | ใช้ในการทดลอง: ยาปฏิชีวนะยับยั้งเนื้องอก |
|
เกลดานามัยซินจะออกฤทธิ์ยับยั้งการทำงานของ Hsp90 (Heat Shock Protein 90) โดยจะเข้าจับกับ ADP/ATP-binding pocket ของโปรตีนแปลกปลอม และขัดขวางการวมตัวกันของ Hsp23 ไปเป็น 90/90- Imph Trimer ซึ่งจะส่งผลต่อการก่อตัวของ HER-2 oncogene ส่วนเฮอร์บิมัยซินจะออกฤทธิ์ลดการเกิดปฏิกิริยาฟอสโฟริเลชันของหมู่ไทโรซีนและลดการทำงานของ Cox-2 แบบจำเพาะเจาะจงโดยไม่มีผลต่อ Cox-1. | |
| เฮอร์บิมัยซิน | Herbamicina A | |||
| คาร์บาซีเฟม | ||||
| ลอราคาร์เบฟ | Lorabid | การติดเชื้อแบคทีเรียในระบบหายใจส่วนบนและการติดเชื้อแบคทีเรียในระบบทางเดินปัสสาวะ | ยับยั้งการสังเคราะห์ผนังเซลล์ของแบคทีเรีย | |
| คาร์บาพีแนม | ||||
| เออร์ตาพีแนม | Invanz | ฆ่าได้ทั้งเชื้อแบคทีเรียแกรมบวกและแกรมลบ จึงนิยมใช้สำหรับการให้ยาปฏิชีวนะแบบครอบคลุมเชื้ออย่างกว้าง (empiric therapy) (Staphylococcus aureus ที่ดื้อต่อเมทิซิลลินจะดื้อต่อยากลุ่มนี้ด้วย) การใช้อีมิพีแนมร่วมกับซิลาสเตตินจะช่วยลดการที่อีมิพีแนมถูกทำให้หมดฤทธิ์โดยเอนไซม์ในร่างกายมุนษย์และช่วยลดความเสี่ยงในการเกิดพิษต่อไต ในกลุ่มนี้เออร์ตาพีแนมจะออกฤทธิ์ต้านแบคทีเรียวงศ์เอนเทอร์โรแบคทีเรียซีอีได้ดีที่สุด |
|
ออกฤทธิ์โดยอาศัยวงบีตา-แลคแตม: ยับยั้งการแบ่งตัวของแบคทีเรียโดยการยับยั้งการสร้างผนังเซลล์ของแบคทีเรีย |
| โดริพีแนม | Finibax | |||
| อีมิพีแนม | ||||
| อีมิพีแนม/ซิลาสเตติน | Primaxina | |||
| มีโรพีแนม | Merrem | |||
| เซฟาโลสปอริน (รุ่นที่ 1) | ||||
| เซฟาดรอกซิล | Duricef | เนื่องจากยาทุกชนิดในกลุ่มเซฟาโลสปอรินนี้มีวงบีตา-แลคแตม จึงมีคุณสมบัติเป็นยาปฏิชีวนะที่ออกฤทธิ์ฆ่าเชื้อแบคทีเรีย (Bacteriacidal agents) เช่นเดียวกันกับกลุ่มเพนิซิลลิน โดยจะออกฤทธิ์ต่อแบคทีเรียแกรมบวกได้ดี เช่น สกุลโปรตีอัส, Escherichia coli และสกุลเคลบซิลลา |
|
ออกฤทธิ์เช่นเดียวกับยาอื่นในกลุ่มบีตา-แลคแตม โดยจะรบกวนการสร้างเปบทิโดไกลแคน ซึ่งเป็นส่วนประกอบที่สำคัญของผนังเซลล์ของแบคทีเรีย ยากลุ่มนี้มีความไวต่อเอนไซม์บีตาแลคตาเมสต่ำ |
| เซฟาโซลิน | Ancef | |||
| เซฟาโลติน | Keflin | |||
| เซฟาเลกซิน | Keflex | |||
| เซฟราดีน | Veracef | |||
| เซฟาโลสปอริน (รุ่นที่ 2) | ||||
| เซฟาคลอร์ | Ceclor | มีประสิทธิภาพมากกว่าเพนิซิลลินในการต้านเชื้อแบคทีเรียแกรมลบรูปแท่ง แต่มีประสิทธิภาพเทียบเท่ากันในการต้านแบคทีเรียแกรมบวกรูปวงกลม โดยยากลุ่มนี้จะออกฤทธิ์ครอบคลุมเชื้อต่อไปนี้ได้ดี แบคทีเรียแกรมบวกรูปวงกลม, Haemophilus influenzae, Enterobacter, Neisseria, Proteus, Escherichia coli และ Klebsiella |
|
ออกฤทธิ์เช่นเดียวกับยาอื่นในกลุ่มบีตา-แลคแตม โดยจะรบกวนการสร้างเปบทิโดไกลแคน ซึ่งเป็นส่วนประกอบที่สำคัญของผนังเซลล์ของแบคทีเรีย |
| เซฟาแมนโดล | Mandol | |||
| เซโฟซิติน | Mefoxitin | |||
| เซฟโปรซิล | Cefzil | |||
| เซฟูรอกซิม | Ceftina, Zinnat | |||
| เซฟาโลสปอริน (รุ่นที่ 3) | ||||
| เซฟิซิม | Suprax | เซฟาโลสปอรินกลุ่มนี้จะใช้ในการรักษาโรคติดเชื้อแบคทีเรียยที่รุนแรงอันเนื่องมาจากเชื้อสาเหตุเป็นเชื้อที่ดื้อต่อยาปฏิชีวนะชนิดอื่นในกลุ่มบีตา-แลคแตม เช่น เยื่อหุ้มสมองอักเสบ เป็นต้น ใช้เป็นยาป้องกันการจิดเชื้อแบคทีเรียก่อนการทำศัลยศาสตร์ออร์โทพีดิกส์ หรือการผ่าตัดบริเวณหน้าท้อง หรืออุ้งเชิงกราน |
|
ออกฤทธิ์เช่นเดียวกับยาอื่นในกลุ่มบีตา-แลคแตม โดยจะรบกวนการสร้างเปบทิโดไกลแคน ซึ่งเป็นส่วนประกอบที่สำคัญของผนังเซลล์ของแบคทีเรีย |
| เซฟดิเนียร์ | Omnicef | |||
| เซฟดิตอเรน | Meiact | |||
| เซโฟเพอราโซน | Cefobid | |||
| เซฟโฟแทกซิม | Claforan | |||
| เซฟโปดอกซิม | Vantin | |||
| เซฟตาซิดิม | Fortaz | |||
| เซฟติบูเตน | Cedax | |||
| เซฟติซอกซีม | Cefizox | |||
| เซฟไตรอะโซน | Rocephin | |||
| เซฟาโลสปอริน (รุ่นที่ 4) | ||||
| เซฟีพิม | Maxipime | ออกฤทธิ์ครอบคลุมสกุล Pseudomonas มากขึ้น รวมถึงแบคทีเรียแกรมบวกด้วย |
|
รบกวนการสร้างเปบทิโดไกลแคน |
| เซฟาคลิดีน | Cefclidin | |||
| เซฟาโลสปอริน (รุ่นที่ 5) | ||||
| เซฟโตบิโพรล | Zevtera | มีฤทธิ์ต้าน Staphylococcus aureus ที่ดื้อต่อเมทิซิลลินได้ดี |
|
รบกวนการสร้างเปบทิโดไกลแคน |
| ไกลโคเปปไทด์ | ||||
| ไทโคพลานิน | Targocid | ใช้สำหรับผู้ป่วยในระยะวิกฤติที่แพ้ต่อยากลุ่มบีตา-แลคแตม | เป็นอาการข้างเคียงที่ผันกลับมาเป็นปกติได้:
|
|
| แวนโคมัยซิน | Vancocin | |||
| แมโครไลด์ | ||||
| อะซิโทรมัยซิน | Zitromax, Sumamed, Zitrocin | การติดเชื้อแบคทีเรียสกุลสเตรปโตคอกคัส, ซิฟิลิส, การติดเชื้อแบคทีเรียในระบบทางเดินหายใจ, การติดเชื้อแบคทีเรียสกุลไมโคพลาสมา, โรคไลม์ | ยับยั้งการสังเคราะห์โปรตีนของแบคทีเรีย โดยจับกับหน่วยย่อย 50 เอสของไรโบโซมแบคทีเรีย | |
| คลาริโทรมัยซิน | Klaricid | |||
| ดิริโทรมัยซิน | Dynabac | |||
| อิริโทรมัยซิน | Eritocina, Eritroped | |||
| ร็อกซิโทรมัยซิน | Roxitrol | |||
| โทรลีแอนโดมัยซิน | (TAO) | |||
| เทลิโทรมัยซิน | Ketek | ปอดบวม | การมองเห็นผิดปกติ, เกิดพิษต่อตับ | |
| สเปคติโนมัยซิน | Trobicin | Antimetabolite, มะเร็ง และหนองใน | ||
| มอนอแบคแตม | ||||
| แอซทรีโอแนม | Azactam | การติดเชื้อแบคทีเรียแกรมลบชนิดใช้ออกซิเจน เช่น วงศ์เอนเทอร์โรแบคทีเรียซีอี และสกุลเยอซิเนีย, สกุลเพลสสิโอโมแนส, สกุลแอโรโมแนส, และสกุลไนซีเรีย ไม่มีผลต่อแบคทีเรียแกรมบวกรูปทรงกลม, แบคทีเรียที่ไม่ใช้ออกซิเจน และสกุลอซีเนโตแบคเตอร์ | ผื่น, ผลการตรวจการตรวจการทำงานของตับผิดปกติ สามารถใช้ยานี้ได้อย่างปลอดภัยในผู้ที่แพ้เพนิซิลลิน | เช่นเดียวกันกับยาอื่นในกลุ่มบีตา-แลคแตม: ยับยั้งการสร้างเปบทิโดไกลแคนของแบคทีเรีย ซึ่งเป็นส่วนประกอบที่สำคัญของผนังเซลล์, จับกับเอนไซม์ Penicillin-binding protein 3 (PBP3) ในแบคทีเรียแกรมลบ |
| เพนิซิลลิน | ||||
| อะม็อกซีซิลลิน | Novamox, Amoxil | ใช้รักษาโรคที่เกิดจากการติดเชื้อได้อย่างหลากหลายขึ้นกับชนิดของยา เช่น การติดเชื้อแบคทีเรียสกุลสเตรปโตคอกคัส, ซิฟิลิส, โรคไลม์ |
|
ช่นเดียวกันกับยาอื่นในกลุ่มบีตา-แลคแตม: ยับยั้งการสร้างเปบทิโดไกลแคนของแบคทีเรีย ซึ่งเป็นส่วนประกอบที่สำคัญของผนังเซลล์ |
| แอมพิซิลลิน | Unasayn | |||
| อะโซลซิลลิน | Securopen | |||
| คาร์เบนิซิลลิน | Pyopen | |||
| คลอกซาซิลลิน | Anaclosil | |||
| ไดคลอกซาซิลลิน | Dicloran | |||
| ฟลูคลอกซาซิลลิน | Floxapen | |||
| เมซโลซิลลิน | Baypen | |||
| เมทิซิลลิน | Staphcillin | |||
| นาฟซิลลิน | Nallpen | |||
| ออกซาซิลลิน | Prostafilina | |||
| เบนซิลเพนิซิลลิน (G) | ||||
| ปิปเปอราซิลลิน | Pipracil | |||
| ไทคาร์ซิลลิน | Timentin | |||
| พอลิเพปไทด์ | ||||
| แบซิทราซิน | การติดเชื้อแบคทีเรียที่ตา, หู, กระเพาะปัสสาวะ โดยปกติมักบริหารยาโดยการทาหรือหยอดลงบนบริเวณที่ติดเชื้อโดยตรง พบเห็นการบริหารยาโดยการฉีดได้น้อยมาก | เกิดพิษต่อไตและระบบประสาท หากบริหารยาโดยการฉีด | ยับยั้งการสร้างเปบทิโดไกลแคนของแบคทีเรีย ซึ่งเป็นส่วนประกอบที่สำคัญของผนังเซลล์ | |
| โคลิสติน | รบกวนการผ่านเข้าออกของสารต่าง ๆ (permeability) ของเซลล์แบคทีเรีย โดยเข้าจับกับเยื่อหุ้มเซลล์ของแบคทีเรีย | |||
| พอลีมิกซิน บี | ||||
| ควิโนโลน | ||||
| ซิโปรฟลอกซาซิน | Cipro, Ciproxin, Ciprobay | การติดเชื้อแบคทีเรียในระบบทางเดินปัสสาวะ, ต่อมลูกหมากอักเสบจากการติดเชื้อแบคทีเรีย, โรคปอดอักเสบชุมชน, ท้องเสียจากการติดเชื้อแบคทีเรีย, การติดเชื้อสกุลไมโคพลาสมา, และหนองใน ยากลุ่มนี้มีผลต่อแบคทีเรียที่ไม่ใช้ออกซิเจนน้อยมาก | คลื่นไส้ (น้อยมาก), เส้นเอ็นอักเสบเรื้อรัง (น้อยมาก) | ยับยั้งเอนไซม์ Topoisomerase, DNA gyrase และเอนไซม์อื่นอีกหลายชนิด, ยับยั้งการถ่ายแบบดีเอ็นเอและการถอดรหัสพันธุกรรม |
| อีนอกซาซิน | Enoxin | |||
| กาติฟลอกซาซิน | Tequin | |||
| ลีโวฟลอกซาซิน | Tavanic | |||
| โลมิฟลอกซาซิน | Loflox | |||
| มอกซิฟลอกซาซิน | Avelox | |||
| นอร์ฟลอกซาซิน | Noroxin | |||
| ออฟลอกซาซิน | Ocuflox | |||
| โทรวาฟลอกซาซิน | Trovan | |||
| ซัลโฟนาไมด์ | ||||
| เมฟีไนด์ | การติดเชื้อแบคทีเรียในระบบทางเดินปัสสาวะ (ยกเว้นซัลฟาซีตาไมด์ และเมฟีไนด์) ; เมฟีไนด์ใช้เป็นยาทาแผลไฟไหม้ |
|
ยับยั้งการสังเคราะห์กรดโฟลิก ซึ่งเป็นสารที่มีความสำคัญต่อการสังเคราะห์ดีเอ็นเอและอาร์เอ็นเอ | |
| พรอนโตซิล (ยาเก่า) | ||||
| ซัลฟาซีตาไมด์ | ||||
| ซัลฟาเมไทโซล | ||||
| ซัลฟานิลาไมด์ (ยาเก่า) | ||||
| ซัลฟาซาลาซีน | ||||
| ซัลฟาฟูราโซล | ||||
| ไตรเมโทพริม | ||||
| ไตรเมโทพริม/ซัลฟาเมโทซาโซล (โคไตรมอกซาโซล หรือ แบคตริม) | ||||
| เตตราไซคลีน | ||||
| เดเมโคลไซคลีน | ซิฟิลิส หรือการติดเชื้อแบคทีเรียที่มีสาเหตุมาจากแบคทีเรียสกุลคลามัยเดีย, สกุลไมโคพลาสมา และสกุลสกุลริคเค็ทเซีย รวมไปถึงสิวที่เกิดจากการติดเชื้อแบคทีเรีย | ยับยั้งการสังเคราะห์โปรตีนของแบคทีเรียโดยการเข้าจับกับหน่วยย่อย 30 เอสของไรโบโซมแบคทีเรีย | ||
| ดอกซีไซคลีน | Vibramicina | |||
| มิโนไซคลีน | Minocin | |||
| ออกซิเตตราไซคลีน | Terramicina | |||
| เตตราไซคลีน | Sumycin | |||
| เอมเฟนิคอล | ||||
| คลอแรมเฟนิคอล | Chloromycetin | มีประสิทธิภาพในการต้านแบคทีเรียทั้งแกรมบวกและแกรมลบ รวมไปถึงพวกที่ไม่ใช้ออกซิเจน | การเกิดพิษองยาจะสัมพันธ์กับขนาดยา โดยอาจเกิดการกดไขกระดูก นำไปสู่การเกิดโรคโลหิตจางจากไขกระดูกฝ่อได้ แต่ส่วนใหญ่สามารถผันกลับเป็นปรกติได้หลังการหยุดใช้ยา | เข้าจับกับหน่วยย่อย 50 เอสของไรโบโซมแบคทีเรียแบบผันกลับได้ ส่งผลให้การสังเคราะห์โปรตีนของแบคทีเรียหยุดชะงักและสิ้นสุดลงเร็วกว่าปกติ |
| อื่น ๆ | ||||
| อาร์สเฟนามิน | Salvarsan | การติดเชื้อแบคทีเรียชั้นสไปโรคีท (เลิกใช้แล้ว) | เกิดพิษจากสารหนู | ปลดปล่อยอนุภาค RAs (OH)2, ออกมา ซึ่งอนุภาคนี้จะก่อให้เกิดพิษต่อแบคทีเรีย Treponema pallidum |
| คลินดามัยซิน | Cleocin | การติดเชื้อเชื้อแบคทีเรียที่ไม่ใช้ออกซิเจน, สิวจากการติดเชื้อแบคทีเรีย, ใช้ป้องกันการติดเชื้อแบคทีเรียของงแผนก่อนทำการผ่าตัด, และใช้กรณีติดเชื้อแบคทีเรีย Staphylococcus aureus ที่ดื้อต่อเมทิซิลลิน (MRSA) | มักพบการเกิดอาการท้องเสียจากการติดเชื้อแบคทีเรีย Clostridium difficile ซึ่งมักนำไปสู่การเกิดภาวะลำไส้ใหญ่อักเสบ Pseudomembranous colitis (PMC) | ยับยั้งการสังเคราะห์โปรตีนของแบคทีเรีย โดยเข้าจับกับหน่วยย่อย 50 เอสของไรโบโซมแบคทีเรีย |
| ลินโคมัยซิน | Lincocin | สิวอักเสบจากการติดเชื้อแบคทีเรีย, ป้องกันการติดเชื้อแบคทีเรียของแผลหลังการผ่าตัด, โรคที่เกิดจากการติดเชื้อแบคทีเรียในไฟลัมแอคติโนมัยสีท, สกุลไมโคพลาสมา และสกุลพลาสโมเดียมบางสายพันธุ์ | ลำไส้ใหญ่อักเสบ ซึ่งในบางรายอาการอาจรุนแรงจนเสียชีวิตได้ | เช่นเดียวกับกลุ่มแมโครไลด์ โดยจะเข้าจับกับหน่วยย่อย 50 เอสของไรโบโซมแบคทีเรีย เพื่อยับยั้งการสังเคราะห์โปรตีน |
| อีแทมบูทอล | Myambutol (ตัวย่อ: EMB) | ยาต้านวัณโรค | ส่วนใหญ่มักเกิดภาวะเส้นประสาทตาอักเสบ ดังนั้นจึงห้ามใช้ในเด็กอายุต่ำกว่า 6 ปี | ยับยั้งการสร้างผนังเซลล์ของแบคทีเรีย |
| ฟอสโฟมัยซิน | Monurol | การติดเชื้อแบคทีเรียในระบบทางเดินปัสสาวะ | อาการไม่พึงประสงค์น้อย ในบางรายอาจมีอาการคลื่นไส้, อาเจียน | ยับยั้งการสร้างผนังเซลล์ของแบคทีเรีย |
| กรดฟูซิดิค | Fucidin | โดยส่วนใหญ่จะออกฤทธิ์ต่อแบคทีเรียแกรมบวก เช่น สกุลสแตฟฟิโลคอคคัส, สกุลสเตรปโตคอกคัส และสกุลโครีนีแบคทีเรียม | ดีซ่าน, ปัสสาวะสีน้ำตาลคล้ำ ทั้งนี้อาการผิดปกติดังกล่าวสามารถกลับคืนเป็นปกติได้หลังจากหยุดใช้ยา | ยับยั้งการสังเคราะห์โปรตีน โดยขัดขวางกระบวนการการนำสารตัวกลางที่ใช้ในการต่อลำดับกรดอะมิโนกลับมาใช้ใหม่ (Elongation factor) |
| ฟูราโซลิโดน | Furoxone | ท้องเสีย และลำไส้เล็กอักเสบที่มีสาเหตุมาจากการติดเชื้อโปรโทซัว, อหิวาตกโรค และเจียอาร์ไดอาซิส | อาการไม่พึงประสงค์ที่พบได้บ่อยคือ สั่น, ไม่สบายท้อง, คลื่นไส้, อาเจียน, เส้นประสาทอักเสบ (neuritis) | สร้างการเชื่อมโยงข้าม (cross-link) กับดีเอ็นเอของแบคทีเรีย |
| ไอโซไนอะซิด | Laniazid | ยารักษาวัณโรค | ชาตามมือ-เท้า, ตับอักเสบ, คลื่นไส้, อาเจียน, ผื่น | ยับยั้งการสังเคราะห์โปรตีนของเชื้อแบคทีเรีย |
| ไลนิโซลิด | Zyvoxid | การติดเชื้อที่มีสาเหตุมาจากแบคทีเรียแกรมบวกที่ดื้อต่อยาปฏิชีวนะชนิดอื่น | ปวดศีรษะ, คลื่นไส้, อาเจียน, ท้องผูก, ปฏิกิริยาการแพ้ยา, ตับอ่อนอักเสบ, และมีการเพิ่มขึ้นของเอนไซม์ทรานซามิเนส โดยความเสี่ยงในการเกิดอาการไม่พึงประสงค์จะเพิ่มมากขึ้นเมื่อใช้ยาในขนาดสูงหรือต่อเนื่องนานเกินไป | ยับยั้งการสังเคราะห์โปรตีนของแบคทีเรีย โดยเข้าจับกับไรโบโซม |
| เมโทรนิดาโซล | Flagyl หรือ Flegyl | โรคที่เกิดจากการติดเชื้อโปรโทซัว และเชื้อแบคทีเรียที่ไม่ใช้ออกซิเจน ซึ่งรวมถึง Bacteroides fragilis, สกุลฟูโซแบคทีเรียม, สกุลเวอิลโลเนลลา, Clostridium difficile และ C. perfringens, สกุลยูแบคทีเรียม, สกุลเพพโทคอคคัส, สกุลไกอาร์เดีย และสกุลเปปโตสเตรปโตคอกคัส | ปัสสาวะสีแดง, การรับรสผิดปกติ, การใช้ยาต่อเนื่องเป็นระยะเวลานานอาจทำให้เกิดปลายประสาทอักเสบได้ | ยับยั้งการสังเคราะห์กรดนิวคลีอิกของแบคทีเรีย โดยทำให้เกิดการแตกออกของดีเอ็นเอ |
| มูพิโรซิน | Bactroban | ออกฤทธิ์กว้าง โดยที่ความเข้มข้นต่ำจะออกฤทธิ์ต้านการเจริญเติบโตของเชื้อแบคทีเรีย แต่จะออกฤทธิ์ฆ่าเชื้อแบคทีเรียเมื่อมีความเข้มข้นสูง | แบคทีเรียดื้อต่อยานี้ได้ง่าย | ยับยั้งการสังเคราะห์โปรตีนของแบคทีเรีย |
| ไนโตรฟูรานโทอิน | Macrodantina, Macrobido | โดยทั่วไปใช้สำหรับรักษาการติดเชื้อแบคทีเรียในระบบทางเดินปัสสาวะ | ส่วนใหญ่มักมีอาการคลื่นไส้, อาเจียน พบการเกิดอาการทางระบบหายใจที่เกี่ยวเนื่องกับการแพ้ยาได้บ้างเล็กน้อย, เกิดพิษต่อระบบทางเดินหายใจ | สร้างความเสียหายแก่ดีเอ็นเอ โดยเฉพาะในรูปที่ถูกรีดิวซ์จะออกฤทธิ์ได้ดี |
| พลาเทนซิมัยซิน | อยู่ในระหว่างการศึกษาทางคลินิก ซึ่งพบว่าออกฤทธิ์ต้านแบคทีเรีย Staphylococcus aureus ที่ดื้อต่อเมทิซิลลิน (MRSA) ในหนูทดลองได้ดี | ยังไม่ทราบแน่ชัด เนื่องจากกำลังอยู่ในขั้นการศึกษาทางคลินิก | ยับยั้งเอนไซม์ beta-ketoacyl synthases I/II (FabF/B) ซึ่งเป็นเอนไซม์หลักที่ทำหน้าเกี่ยวกับการสังเคราะห์กรดไขมันที่เป็นส่วนประกอบของเยื่อหุ้มเซลล์ของแบคทีเรีย | |
| ไพราซินาไมด์ | ตัวย่อ: PZA | ยารักษาวัณโรค | ปวดตามข้อ แต่ส่วนใหญ่อาการมักไม่รุนแรง, ตับอักเสบ, คลื่นไส้, อาเจียน, เบื่ออาหาร, ผื่น | ยับยั้งเอนไซม์ Fatty acid synthase (FAS) ซึ่งทำหน้าที่ในการสังเคราะห์กรดไขมันที่เป็นส่วนประกอบของเยื่อหุ้มเซลล์แบคทีเรีย |
| ควินูปริสติน/ดาลโฟปริสติน | Synercid | สกุลสแตฟฟิโลคอคคัส และ Enterococcus faecium ที่ดื้อต่อยาแวนโคมัยซิน | ปวดในข้อ, คลื่นไส้, อาเจียน, ท้องเสีย, ผื่น, คัน, ปวดศีรษะ,หลอดเลือดดำอักเสบ, ภาวะบิลิรูบินในเลือดสูง นอกจากนี้ยังส่งผลยับยั้งการทำงานของระบบเอนไซม์ไซโทโครม P450 (CYP 450) | ยับยั้งการสังเคราะห์โปรตีนของแบคทีเรีย โดยยาทั้งสองจะเสริมฤทธิ์กันดาลโฟปริสติน จะเข้าจับกับยูนิตย่อย 23 เอสของหน่วยย่อย 50 เอสบนไรโบโซมของแบคทีเรีย ส่งผลให้รูปร่างของไรโบโซมเปลี่ยนไป และช่วยให้ควินูปริสตินเข้าจับกับหน่วยย่อย 50 เอสบนไรโบโซมได้มากขึ้น ซึ่งจะยับยั้งการต่อสายพอลิเปปไทด์ |
| ไรแฟมพิซิน หรือ ไรแฟมพิน | Rifaldin | รักษาโรคเรื้อน, วัณโรค และโรคลีเจียนเนลโลสิส โดยใช้ร่วมกับยาปฏิชีวนะอื่น ยกเว้นในกรณีเพื่อป้องกันการติดเชื้อ Haemophilus influenzae ชนิด บี และไข้กาฬหลังแอ่น ในผู้ที่มีความเสี่ยงต่อโรคดังกล่าว | คลื่นไส้, อาเจียน, ท้องเสีย หรือ ไม่อยากอาหาร น้ำปัสสาวะและเหงื่อเป็นสีแดงออกส้ม ตับอักเสบ และยังอาจก่อให้เกิดการแพ้ยาได้ | ขัดขวางการสร้างอาร์เอ็นเอของแบคทีเรีย ผ่านการยับยั้งการทำงานของเอนไซม์ DNA-dependent RNA polymerase ของแบคทีเรีย |
| ทินิดาโซล | Fasigyn, Simplotan, Tindamax | ท่อปัสสาวะอักเสบ, ภาวะช่องคลอดอักเสบ, บิดมีตัว และเจียอาร์ไดอาซิส | ง่วงซึม, ปวดศีรษะ, มึนงง หากรับประทานพร้อมเครื่องดื่มแอลกอฮอล์จะทำให้เกิดกลุ่มอาการคล้ายปฏิกิริยาจากยาไดซัลฟิแรม (Disulfiram-like Reaction) ได้ เช่น คลื่นไส้ อาเจียน ปวดศีรษะ ความดันโลหิตสูงขึ้น หน้าแดง หายใจหอบเหนื่อย เป็นต้น | ปลดปล่อยอนุมูลอิสระที่เป็นพิษต่อเซลล์ปรสิต |
| ชื่อสามัญทางยา | ชื่อการค้า | ข้อบ่งใช้ | อาการไม่พึงประสงค์ | กลไกการออกฤทธิ์ |
การผลิต
ด้วยความก้าวหน้าทางเภสัชเคมี ทำให้ยาปฏิชีวนะที่มีใช้อยู่ทุกวันนี้สามารถผลิตได้จากวิธีการกึ่งสังเคราะห์ โดยการดัดแปลงสูตรโครงสร้างของสารประกอบจากธรรมชาติที่มีฤทธิ์ต้านแบคทีเรียให้มีความเหมาะสมในการใช้กับมนุษย์มากขึ้น ตัวอย่างที่เห็นได้อย่างชัดเจนคือ ยาปฏิชีวนะจำพวกบีตา-แลคแตม ซึ่งกลุ่มเพนิซิลลิน (ผลิตจากราในสกุลเพนิซิลเลียม), กลุ่มเซฟาโลสปอริน, และกลุ่มคาร์บาพีแนม ก็ล้วนแต่ถูกจัดอยู่ในยาปฏิชีวนะจำพวกนี้ ส่วนยาปฏิชีวนะที่ใช้ในปัจจุบันที่ต้องสกัดจากจุลชีพที่มีชีวิตเท่านั้น คือ ยาปฏิชีวนะในกลุ่มอะมิโนไกลโคไซด์ ส่วนกลุ่มอื่น ๆ นั้นล้วนได้มาจากการสังเคราะห์ในห้องปฏิบัติการ เช่น ซัลโฟนาไมด์, ควิโนโลน, ออกซาโซลิไดโอน เป็นต้น ยาปฏิชีวนะโดยส่วนใหญ่มักมีขนาดโมเลกุลที่ค่อนข้างเล็กและมีมวลโมเลกุลน้อยกว่า 1000 ดาลตัน
การที่เอินซต์ เชนและฮาเวิร์ด ฟลอเรย์สามารถสกัดเพนิซิลลินบริสุทธิ์เพื่อใช้ในมนุษย์ได้สำเร็จใน ค.ศ. 1941 ทำให้ยาดังกล่าวถูกผลิตขึ้นให้กับกองทัพเพื่อใช้รักษาผู้บาดเจ็บฝ่ายสัมพันธมิตรในระหว่างการทำสงครามโลกครั้งที่ 2 เป็นจำนวนมาก จนทำให้การผลิตที่ประเทศอังกฤษนั้นไม่สามารถสนับสนุนความต้องการในการใช้ยานี้ได้อย่างเพียงพอ จึงได้มีการย้ายฐานการผลิตไปยังสหรัฐอเมริกา ซึ่งมีกำลังการผลิตที่มากกว่า จนกระทั่งสงครามโลกครั้งที่ 2 สิ้นสุดลง จึงได้มีการผลิตเพนิซิลลินออกสู่ตลาดยาสาธารณะ อย่างไรก็ตาม ถึงแม้ว่ายาปฏิชีวนะที่มีอยู่ในตลาดยาทุกวันนี้ส่วนใหญ่จะได้มาจากการสังเคราะห์ของจุลชีพ (เช่น เพนิซิลลิน) แต่ด้วยความก้าวหน้าของเทคโนโลยีชีวภาพทำให้สามารถเพิ่มศักยภาพการผลิตได้มากขึ้น จนสามารถผลิตในเชิงการค้าได้ในที่สุด ด้วยความก้าวนี้ทำให้สามารถผลิตเพนิซิลลินได้มากกว่าวิธีการสกัดแรกเริ่มของเฟลมมิงถึง 40000 เท่า ต่อมาในช่วงปลายทศวรรษที่ 1960 นักวิจัยพบว่าแบคทีเรียที่ผลิตเพนิซิลลินนั้นสามารถเจริญได้ดีในสภาวะที่ไม่มีออกซิเจน การค้นพบนี้ทำให้ศักยภาพการผลิตเพนิซิลลินเพิ่มขึ้นอีกถึง 200 %
หลังจากการค้นพบเพนิซิลลินเพียงไม่กี่ปี พบว่ายาดังกล่าวเป็นที่นิยมและแพร่หลายเป็นอย่างมาก โดยในปี ค.ศ. 1945 มีการผลิตเพนิซิลลินขึ้นมากถึง 646 พันล้านยูนิต แต่ต่อมาหลังมีการพัฒนายากลุ่มดังกล่าวจนได้เป็นยากลุ่มเซฟาโลสปอริน ทำให้แนวโน้มการใช้ยาปฏิชีวนะนั้นโน้มเอียงมาทางยากลุ่มนี้มากขึ้น โดยในปี ค.ศ. 1980 ยากลุ่มเซฟาโลสปอรินเป็นยาปฏิชีวนะที่ถูกผลิตขึ้นเชิงการค้ามากที่สุด ตามมาด้วยแอมพิซิลลิน และเตตราไซคลีน ตามลำดับ เป็นที่คาดการณ์กันว่าในปีนั้นมีการผลิตยาปฏิชีวนะในปริมาณรวมมากถึง 100 ล้านกิโลกรัม มูลค่าการซื้อขายเฉพาะยาปฏิชีวนะในสหรัฐอเมริกาในปีนั้นมีมากถึง 1000 ล้านดอลลาร์สหรัฐ ส่วนมูลค่าทางการตลาดของยาปฏิชีวนะทั้งหมดในปัจจุบันนั้นมีมูลค่าประมาณ 20000 ล้านดอลลาร์สหรัฐ ทั้งนี้ ในการคิดค้นและพัฒนายาปฏิชีวนะชนิดใหม่เข้าสู่ตลาดยาในปัจจุบันนั้นต้องใช้งบประมาณประมาณ 1200 ล้านดอลลาร์สหรัฐ แต่ด้วยมูลค่าทางการตลาดที่มหาศาลของยาปฏิชีวนะชนิดหนึ่ง ๆ ทำให้ธุรกิจด้านการคิดค้นพัฒนายาชนิดนี้ออกจำหน่ายในตลาดยานั้นมีการแข่งขันกันเป็นอย่างมาก โดยการดำเนินงานวิจัยเพื่อคิดค้นและพัฒนายาใหม่ในปัจจุบันมักเป็นการดำเนินงานโดยบริษัทที่เน้นการดำเนินธุรกิจจัดจำหน่ายเคมีภัณฑ์และโภคภัณฑ์ (Commodity chemical) เป็นส่วนมาก
การผลิตยาปฏิชีวนะเชิงอุตสาหกรรมจากจุลชีพนั้นจะใช้กระบวนการการหมัก ซึ่งจุลชีพเหล่านั้นจะถูกเพาะเลี้ยงในหม้อคอลดรอนขนาดใหญ่ (ปริมาตรประมาณ 100000–150000 ลิตรต่อหม้อ) ซึ่งภายในจะบรรจุอาหารเลี้ยงเชื้อที่จำเพาะต่อจุลชีพสายพันธุ์นั้น ๆ โดยจะมีการควบคุมสภาวะต่าง ๆ อาทิ ความเข้มข้นของออกซิเจน อุณหภูมิ ค่าพีเอช และระดับสารอาหาร ให้มีเหมาะสมต่อการเจริญเติบโตของจุลชีพที่ใช้ในกระบวนการผลิต ส่วนยาปฏิชีวนะซึ่งเป็นสารเมตาบอไลต์ของจุลชีพนั้นจะถูกสกัดออกมาให้บริสุทธิ์และทำให้ตกผลึก ทั้งนี้ขั้นตอนและกระบวนการสกัดยาปฏิชีวนะให้บริสุทธิ์จะขึ้นอยู่กับสมบัติทางเคมีของยานั้น ๆ ตัวอย่างกระบวนการที่ใช้ในการผลิต เช่น การแลกเปลี่ยนไอออน, การตกตะกอน เป็นต้น โดยจุลินทรีย์ที่ได้รับการศึกษาเพื่อการสร้างยาปฏิชีวนะมากที่สุดคือแบคทีเรียสกุลสเตรปโตมัยซิส กว่า 77 สายพันธ์ของแบคทีเรียในสกุลนี้ได้รับการตกแต่งสารพันธุกรรมบนไรโบโซมเพื่อสร้างยาปฏิชีวนะชนิดใหม่ขึ้นมา
ความสำคัญทางการแพทย์ของยาต้านจุลชีพ ซึ่งรวมไปถึงยาปฏิชีวนะนั้น ได้นำมาซึ่งการค้นคว้าวิจัยเพื่อคิดค้นพัฒนายาปฏิชีวนะชนิดใหม่อย่างกว้างขวางและเข้มข้น ทำให้เกิดพยายามที่จะพัฒนายาปฏิชีวนะชนิดใหม่ที่สามารถออกฤทธิ์ครอบคลุมเชื้อก่อโรคได้เป็นวงกว้างมากขึ้น, มีการปรับเปลี่ยนขนาดภาคการผลิตยาปฏิชีวนะโดยใช้กระบวนการหมักเชื้อในเชิงอุตสาหกรรมเพิ่มมากขึ้น จากความพยามดังข้างต้นของนักวิจัย ทำให้จำนวนยาปฏิชีวนะที่ถูกค้นพบมีจำนวนเพิ่มขึ้นอย่างรวดเร็วจาก 500 ชนิดในทศวรรษที่ 1960 เป็นมากกว่า 11000 ชนิดในปี ค.ศ. 1994 โดยกว่าร้อยละ 50 ของยาปฏิชีวนะเหล่านี้ได้มาจากการสังเคราะห์ของแบคทีเรียสกุลสเตรปโตมัยซิส ส่วนจุลชีพสายพันธุ์อื่นที่มีความสำคัญในการผลิตยาปฏิชีวนะ ได้แก่ ราเส้นใย และแอคติโนมัยสีทสายพันธุ์อื่นที่นอกเหนือจากสกุลสเตรปโตมัยซิส
การตกค้างของยาปฏิชีวนะ
การใช้ยาปฏิชีวนะในปศุสัตว์เป็นสิ่งจำเป็นเนื่องจากต้องมีการป้องกันและรักษาโรคติดเชื้อแบคทีเรียที่เกิดขึ้นกับสัตว์เหล่านั้น การค้นพบการประยุกต์ใช้ยาปฏิชีวนะและวัคซีนบางชนิดในปศุสัตว์นี้ทำให้การเลี้ยงวัวในปริมาณมากนั้นมีความสะดวกมากขึ้น เนื่องจากกระบวนการดังกล่าวจะลดการเกิดโรคติดเชื้อในสัตว์ การใช้ยาปฏิชีวนะในกรณีนี้ทำให้ปศุสัตว์นั้นมีการเจริญเติบโตที่เร็วมากขึ้น ให้ผลผลิตที่มีคุณภาพและปริมาณมากขึ้น อย่างไรก็ตาม การใช้ยาปฏิชีวนะในการปศุสัตว์นี้ทำให้เกิดการตกค้างของยาปฏิชีวนะในผลิตภัณฑ์ต่าง ๆ ซึ่งอาจนำไปสู่การเกิดอันตรายแก่มนุษย์ได้ อาทิ การสะสมของสารหนูซึ่งเป็นส่วนประกอบหนึ่งของโมเลกุลยาปฏิชีวนะบางชนิดในร่างกายมนุษย์ ซึ่งรวมไปถึงการลดทอนประสิทธิภาพการรักษาโรคติดเชื้อแบคทีเรียในมนุษย์ลง ซึ่งเป็นผลเนื่องมาจากการปรับตัวของแบคทีเรียก่อโรคให้ทนต่อยาปฏิชีวนะมากขึ้น ดังนั้น ในปัจจุบัน การตรวจสอบการตกค้างยาปฏิชีวนะตกค้างในผลิตภัณฑ์จากการปศุสัตว์อย่างเข้มข้นและต่อเนื่องจึงเป็นมาตรการสำคัญที่ช่วยรับประกันความปลอดภัยของสินค้าจากการปศุสัตว์นั้นๆได้ก่อนส่งถึงมือผู้บริโภค นอกจากนี้การใช้ยาปฏิชีวนะในการปศุสัตว์ยังเป็นอีกสาเหตุหนึ่งที่ทำให้เกิดการตกค้างของยาปฏิชีวนะในสิ่งแวดล้อมจากการปล่อยของเสียจากสัตว์ลงสู่พื้นดิน หรือแหล่งน้ำธรรมชาติ เช่น แม่น้ำ ทะเลสาบ เป็นต้น
การดื้อยาของจุลชีพ
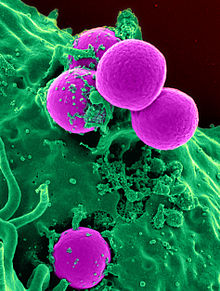
การดื้อต่อยาปฏิชีวนะของแบคทีเรียนั้นเป็นภาวะฉุกเฉินภาวะฉุกเฉินที่พบเกิดขึ้นทั่วทุกมุมโลกในปัจจุบัน โดยการดื้อต่อยาปฏิชีวนะของแบคทีเรียเป็นการตอบสนองและการปรับตัวเพื่อความอยู่รอดในขณะที่มีการใช้ยาปฏิชีวนะเพื่อกำจัดเชื้อแบคทีเรียนั้น ๆ โดยการดื้อยานี้อาจเกิดจากการปรับตัวทางกายภาพหรือทางพันธุกรรมของแบคทีเรียนั้นก็ได้ ซึ่งจะช่วยเพิ่มโอกาสในการอยู่รอดของเชื้อเพิ่มขึ้นแม้จะมีการใช้ยาปฏิชีวนะในขนาดที่สูงขึ้นก็ตาม ในบางสภาวะการใช้ยาปฏิชีวนะอาจทำให้เกิดการเจริญเติบโตของแบคทีเรียดื้อมากขึ้น ในขณะที่แบคทีเรียซึ่งยังมีความไวต่อยาถูกกำจัดออกไป ตัวอย่างเช่น การใช้ยาปฏิชีวนะในการคัดแยกสายพันธุ์แบคทีเรียที่ได้รับการตกแต่งพันธุกรรมด้วยยีนดื้อยาในปี ค.ศ. 1943 โดยเรียกการทดลองนี้ว่า การทดลองของเดลบรัค–ลูเรีย (Luria–Delbrück experiment) สถานการณ์การดื้อต่อยาปฏิชีวนะของแบคทีเรียในปัจจุบันนี้พบว่า ยาปฏิชีวนะหลายชนิดที่มีประสิทธิภาพในการต้านเชื้อแบคทีเรียหลากหลายสายพันธุ์ในอดีต เช่น เพนิซิลลิน และอิริโทรมัยซิน กลับมีประสิทธิภาพในการรักษาโรคติดเชื้อแบคทีเรียต่าง ๆ ได้น้อยลง ทั้งนี้เนื่องมาจากอัตราการดื้อต่อยาปฏิชีวนะของแบคทีเรียมีเพิ่มขึ้นมากกว่าในอดีต
การดื้อต่อยาปฏิชีวนะของแบคทีเรียอาจเกิดขึ้นได้รูปแบบการย่อยสลายทางชีวภาพของยาปฏิชีวนะ ดังเช่นในกรณีของแบคทีเรียในดินที่ทำหน้าที่ย่อยสลายซัลฟาเมทาซีน ซึ่งได้รับซัลฟาเมทาซีนที่ปนเปื้อนออกมากับอุจจาระของหมู โดยการปรับตัวให้อยู่รอดจากยาปฏิชีวนะได้นี้ส่วนใหญ่แล้วมักเกิดถ่ายทอดทางพันธุกรรมได้ แต่ในกรณีการเจริญเติบโตของแบคทีเรียที่ดื้อต่อยาปฏิชีวนะนั้นมักเกิดจากการที่แบคทีเรียหนึ่ง ๆ ได้รับยีนต้านทานยาปฏิชีวนะมาจากแบคทีเรียเซลล์อื่น (horizontal gene transfer) โดยกระบวนการถ่ายทอดยีนนี้มักเกิดขึ้นได้บ่อยในพื้นที่ที่มีการใช้ยาปฏิชีวนะสูง
ข้อมูลที่ได้จากการศึกษาทางโบราณคดีพบว่าการดื้อต่อยาปฏิชีวะในแบคทีเรียนั้นเป็นกลไกที่พบเกิดขึ้นได้ตั้งแต่สมัยโบราณ ทำให้เกิดการกลายพันธุ์ของเชื้อแบคทีเรียจนได้เป็นสายพันธุ์ที่ทนสารที่ออกฤทธิ์เป็นยาปฏิชีวนะที่เคยใช้ได้ผลในการยับยั้งการสืบพันธุ์และการดำรงชีวิตของแบคทีเรียนั้น ๆ ในอดีต
กลไกการดื้อต่อยาปฏิชีวนะของแบคทีเรียในระดับโมเลเท่าที่ทราบในปัจจุบันนั้น การดื้อยาต่อยาปฏิชีวนะของแบคทีเรียตั้งแต่กำเนิด (Intrinsic resistance) อาจจะเป็นส่วนหนึ่งของการเปลี่ยนแปลงสารพันธุกรรม (genetic makeup) ของแบคทีเรียสายพันธ์นั้น ตัวอย่างเช่น ตำแหน่งที่เป็นเป้าหมายการออกฤทธิ์ของยาปฏิชีวนะอาจจะหายไปจากจีโนมของแบคทีเรีย ส่วนการดื้อต่อยาปฏิชีวนะของแบคทีเรียที่เกิดภายหลัง (Acquired resistance) นั้นจะเป็นผลมาจากการกลายพันธุ์ในโครโมโซมของแบคทีเรีย หรือการได้รับยีนดื้อยาจากแบคทีเรียอื่นผ่านทางดีเอ็นเอที่อยู่นอกโครโมโซม (extra-chromosomal DNA) ทั้งนี้ ในแบคทีเรียบางสายพันธุ์ที่สามารถผลิตสารที่ออกฤทธิ์เป็นยาปฏิชีวนะได้นั้นจะสามารถดื้อต่อยาปฏิชีวนะดังกล่าวได้อย่างอัตโนมัตและอาจมีการถ่ายทอดความสามารถในการดื้อต่อยาปฏิชีวนะนี้ไปยังแบคทีเรียอื่น ๆ ได้เช่นกัน การแพร่กระจายของแบคทีเรียที่ดื้อต่อยาปฏิชีวนะนั้นส่วนใหญ่จะพบในรูปแบบถ่ายทอดพันธุกรรมจากรุ่นสู่รุ่นหรือการติดต่อตามแนวดิ่ง (vertical transmission) และโดยการรวมตัวกันใหม่ของยีน (Genetic Recombination) ในดีเอ็นเอโดยการถ่ายทอดยีนในแนวราบ (Horizontal gene transfer) โดยแบคทีเรียดื้อยาสามารถถ่ายทอดยีนดื้อยาที่ถูกบรรจุอยู่ในพลาสมิดไปยังสเตรนอื่นหรือสายพันธุ์อื่นได้ โดยพลาสมิดบางชนิดที่บรรจุยีนดื้อยาที่แตกต่างกันไว้หลายยีนสามารถทำให้แบคทีเรียที่ดื้อต่อยาปฏิชีวนะหลายขนานได้ โดยการดื้อยาปฏิชีวนะข้ามชนิดหนือข้ามกลุ่มกันในเชื้อแบคทีเรียนั้นอาจพบเกิดขึ้นได้ในกรณีที่กลไกการดื้อต่อยาเหล่านั้นถูกควบคุมโดยยีนตำแหน่งเดียวกัน
ในปัจจุบัน โรคที่เกิดจากการติดเชื้อแบคทีเรียสายพันธุ์หรือสเตรนที่ดื้อต่อยาปฏิชีวนะ หรือในบางครั้งอาจเรียกว่า ซูเปอร์บั๊ก (superbugs) เป็นโรคที่การสาธารณสุขทั่วโลกต่างเห็นพ้องว่าเป็นโรคที่ต้องมีการควบคุมโรคเป็นอย่างดี เนื่องจากอาจเกิดการแพร่กระจายและเกิดการติดต่อเป็นวงกว้างได้ ยกตัวอย่างเช่นภาวะฉุกเฉินที่เกิดจากวัณโรคที่ดื้อต่อยาต้านวัณโรคหลายขนาน (Multidrug-resistant tuberculosis; MDR-TB) ซึ่งเชื้อแบคทีเรียสาเหตุดังกล่าวนั้นดื้อต่อยาต้านวัณโรคหลายชนิดที่เคยมีประสิทธิภาพดีในการรักษาวัณโรคหลายอดีต โดยในทุก ๆ ปีจะมีผู้ป่วยรายใหม่มากกว่าครึ่งล้านที่เจ็บป่วยจากการติดเชื้อวัณโรคที่ดื้อต่อยาปฏิชีวนะหลายขนานสายพันธุ์ โดยกลไกการดื้อยาดังกล่าวนั้นเกิดได้จากหลากหลายกลไก การศึกษาทางคลินิกในปัจจุบันพบว่าเอนไซม์ NDM-1 เป็นเอนไซม์ที่สำคัญอีกชนิดหนึ่งที่ชักนำให้แบคทีเรียเกิดการดื้อต่อยาปฏิชีวนะในกลุ่มบีตา-แลคแตมได้หลายชนิดสำนักงานคุ้มครองสุขภาพ (Health Protection Agency) ของสหราชอาณาจักร ได้ให้ถ้อยแถลงไว้ว่า แบคทีเรียที่มีการสร้างเอนไซม์ NDM-1 ซึ่งคัดแยกได้จากสารคัดหลั่งของผู้ป่วยนั้นดื้อต่อยาปฏิชีวนะรูปแบบฉีดในสูตรการรักษามาตรฐานทุกชนิดของการรักษาโรคติดเชื้อแบคทีเรียที่รุนแรง ในวันที่ 26 พฤษภาคม ค.ศ. 2016 ได้มีการรายงานถึงการพบแบคทีเรียสายพันธุ์ Escherichia coli ที่ดื้อต่อโคลิสตินเป็นครั้งแรกในสหรัฐอเมริกา ซึ่งยาดังกล่าวนั้นถือได้ว่าเป็น “ยาที่ถูกเลือกใช้เป็นอันดับสุดท้าย” (Drug of last resort) หรือยาทางเลือกสุดท้ายที่มีใช้ในกรณีที่ภาวะติดเชื้อนั้นไม่สามารถบำบัดรักษาได้ด้วยยาปฏิชีวนะชนิดอื่น หรือเฉพาะโรคที่เกิดจากการติดเชื้อแบคทีเรียที่ดื้อต่อยาปฏิชีวนะหลายขนาน
การใช้ยาปฏิชีวนะในทางที่ผิด

หลักการสำคัญในการตัดสินใจเลือกใช้ยาปฏิชีวนะเมื่อเกิดการเจ็บป่วยนั้น อย่างง่ายคือ หลีกเลี่ยงการใช้ยาปฏิชีวนะถ้าไม่จำเป็น และหากมีความจำเป็นต้องใช้ยาดังกล่าวก็ไม่ควรที่จะใช้ในจำนวนที่มากเกินจำเป็นเนื่องจากในปัจจุบันการใช้ยาปฏิชีวนะที่ไม่เหมาะสมกับภาวะการเจ็บป่วยหรือใช้มากเกินจำเป็นถือเป็นปัจจัยสำคัญที่ก่อให้เกิดการดื้อต่อยาปฏิชีวนะของแบคทีเรีย ซึ่งถือเป็นอีกประเด็นหนึ่งที่ถูกจัดเป็นภาวะฉุกเฉินทางการแพทย์ในปัจจุบัน ตัวอย่างที่พบเห็นได้ทั่วไปของการใช้ยาปฏิชีวนะที่ไม่เหมาะสมก็คือ การจัดหายาปฏิชีวนะมาใช้เองโดยปราศจากการวินิจฉัยหรือการดูแลที่เหมาะสมจากแพทย์ อย่างไรก็ตาม การสั่งใช้ยาปฏิชีวนะจากบุคลการทางการแพทย์แก่ผู้ป่วยที่เจ็บป่วยด้วยโรคหรืออาการที่ไม่อาจตอบสนองต่อการรักษาด้วยยาปฏิชีวนะ รวมไปถึงโรคหรืออาการบางชนิดที่อาจหายได้เองโดยไม่จำเป็นต้องได้รับการรักษาด้วยยาใด ๆ และการใช้ยาปฏิชีวนะเพื่อรักษาโรคที่เกิดจากการติดเชื้อแบคทีเรียในขนาดหรือระยะเวลาที่ต่ำเกินกว่าที่แนะนำในแบบแผนการรักษามาตรฐาน ล้วนแล้วแต่เป็นสาเหตุที่ก่อให้เกิดการดื้อต่อยาปฏิชีวนะของแบคทีเรียได้ทั้งสิ้น โดยการใช้ยาปฏิชีวนะเกินความจำเป็น อย่างเช่นในกรณีของเพนิซิลลินและอิริโทรมัยซินนั้น พบว่ามีความสัมพันธ์ภาวะฉุกเฉินด้านการดื้อต่อยาปฏิชีวนะของแบคทีเรียมาตั้งแต่คริสต์ทศวรรษที่ 1950 รวมไปถึงการที่มีการใช้ยาปฏิชีวนะในสถานพยาบาลต่าง ๆ อย่างแพร่หลายก็ล้วนมีความสัมพันธ์กับการเกิดการดื้อต่อยาปฏิชีวนะและการเพิ่มขึ้นของจำนวนสายพันธุ์และสเตรนของแบคทีเรียเช่นกัน ซึ่งการดื้อยาของแบคทีเรียนี้เป็นสาเหตุให้โรคติดเชื้อแบคทีเรียหลายชนิดไม่อาจสามารถรักษาได้ด้วยยาปฏิชีวนะทั่วไปในปัจจุบัน
นอกเหนือจากประเด็นดังข้างต้นแล้ว การใช้ยาปฏิชีวนะเกินความจำเป็นสำหรับการป้องกันโรคติดเชื้อแบคทีเรีย และความผิดพลาดในการสั่งใช้และกำหนดขนาดยาปฏิชีวนะให้กับผู้ป่วยของบุคลากรทางการแพทย์ โดยอิงข้อมูลจากคุณลักษณะพื้นฐานและประวัติการรักษาของผู้ป่วยแต่ละราย ก็ล้วนแล้วแต่เป็นสาเหตุของการเกิดการดื้อต่อยาปฏิชีวนะของแบคทีเรียที่พบเห็นได้เป็นประจำ ส่วนสาเหตุอื่นที่อาจพบได้ อาทิ การที่ผู้ป่วยรับประทานยาไม่ครบจำนวนวันตามที่ได้รับการสั่งใช้ยาจากแพทย์ การที่ผู้ป่วยรับประทานยาไม่ได้ขนาดและมีวิธีการบริหารยาที่ไม่ตรงตามที่มีการสั่งใช้ยา หรือการที่ไม่สามารถพักฟื้นได้เพียงพอหลังการรักษา นอกจากนี้การใช้ยาปฏิชีวนะไม่ตรงตามข้อบ่งใช้อย่างการใช้ยาดังกล่าวในการรักษาโรคที่เกิดจากการติดเชื้อไวรัส เช่น โรคหวัด ก็เป็นสาเหตุสำคัญอีกประการหนึ่งที่นำไปสู่การเกิดภาวะฉุกเฉินด้านการดื้อยาของแบคทีเรียได้ โดยการศึกษาหนึ่งพบว่า แพทย์มักสั่งจ่ายยาปฏิชีวนะให้แก่ผู้ป่วยที่มีความต้องการที่จะใช้ยาดังกล่าว ถึงแม้ว่าการสั่งใช้ยานี้จะไม่ตรงตามข้อบ่งใช้ก็ตาม จึงอาจถือได้ว่า การกำหนดมาตรการป้องกันการใช้ยาปฏิชีวนะที่ไม่ตรงตามข้อบ่งใช้ทั้งในด้านการสั่งใช้ยาของแพทย์และการรับรู้ของผู้ป่วยนั้นเป็นปัจจัยสำคัญที่จะช่วยลดการใช้ยาปฏิชีวนะที่ไม่เหมาะสมลงได้
การดื้อต่อยาปฏิชีวนะของแบคทีเรียในปัจจุบันกำลังอยู่ในความสนใจขององค์กรที่เกี่ยวเนื่องกับระบบสาธารณสุขหลายองค์กร ดดยองค์กรเหล่านั้นได้พยายามผลักดันให้มีการบังคับใช้มาตรการต่าง ๆออกมาอย่างต่อเนื่องเพื่อลดปริมาณการใช้ยาปฏิชีวนะที่ไม่สมเหตุสมผล โดยประเด็นการใช้ยาปฏิชีวนะไปในทางที่ผิดและการใช้ยาปฏิชีวนะเกินความจำเป็นได้ถูกบรรจุให้เป็นประเด็นสำคัญในถ้อยแถลงการก่อตั้งหน่วยเฉพาะกิจร่วมด้านการดื้อต่อยาปฏิชีวนะของแบคทีเรียแห่งประเทศสหรัฐอเมริกา โดยหน่วยเฉพาะกิจนี้มีวัตถุประสงค์ในการจัดการและแก้ไขปัญหาดังข้างต้นเป็นหลัก โดยอาศัยความร่วมมือหลักจากองค์กรที่เกี่ยวเนื่อง 3 องค์กร คือ ศูนย์ควบคุมและป้องกันโรค (Centers for Disease Control and Prevention; CDC) องค์การอาหารและยา (Food and Drug Administration; FDA) และสถาบันสุขภาพแห่งชาติ (National Institutes of Health;NIH) รวมไปถึงหน่วยงานอื่นที่เกี่ยวเนื่องอีกหลายหน่วยงาน นอกจากนี้ยังมีโครงการ Keep Antibiotics Working ซึ่งริเริ่มโดยกลุ่มองค์การนอกภาครัฐ เพื่อประชาสัมพันธ์ให้ประชาชนตระหนักถึงอันตรายของแบคทีเรียที่ดื้อต่อยาปฏิชีวนะ ส่วนในฝรั่งเศส ได้มีการริเริ่มโครงการ Antibiotics are not automatic โดยหน่วยงานภาครัฐขึ้นใน ค.ศ. 2002 และนำไปสู้การลดลงของการสั่งใช้ยาปฏิชีวนะโดยไม่จำเป็นได้ในที่สุด โดยเฉพาะอย่าง การใช้ยากลุ่มดังกล่าวในผู้ป่วยวัยเด็ก
ภาวะฉุกเฉินทางการแพทย์ด้านการดื้อยาปฏิชีวนะของแบคทีเรียนั้นส่งผลให้การใช้ยาปฏิชีวนะในสหราชอาณาจักรมีความเข้มงวดมากขึ้นตั้งแต่ปี ค.ศ. 1970 (ตามรายงานของ Swann ระบุว่าเริ่มใน ค.ศ. 1969) และสหภาพยุโรปได้ประกาศห้ามใช้ยาปฏิชีวนะเป็นสารช่วยส่งเสริมการเจริญเติบโต (growth-promotional agent) ในปี ค.ศ. 2003 นอกจากนี้ องค์กรและหน่วยงานด้านสุขภาพหลายองค์กร (รวมถึงองค์การอนามัยโลก สถาบันวิทยาศาสตร์แห่งชาติ และองค์การอาหารและยาของสหรัฐอเมริกา) ได้เข้ามาส่วนสนับสนุนในการจำกัดปริมาณการใช้ยาปฏิชีวนะในการเพาะเลี้ยงปศุสัตว์เพื่อการบริโภค อย่างไรก็ตาม การดำเนินการนี้ต้องล่าช้าลงในขั้นตอนของการร่างกฎหมายและการดำเนินการตามขั้นตอนต่าง ๆ ทางกฎหมายเพื่อจำกัดการใช้ยาปฏิชีวนะในอุตสาหกรรมดังกล่าว เนื่องมาจากต้องเผชิญแรงต้านจากหน่วยงานเอกชนที่ใช้หรือจำหน่ายยาปฏิชีวนะที่ต้องอยู่ภายใต้การกำกับดูแลของภาครัฐ และจำเป็นต้องใช้เวลาในการศึกษาวิจัยเพิ่มเติมเพื่อยืนยันให้ได้แน่ชัดว่าการใช้ยาปฏิชีวนะในอุตสาหกรรมปศุสัตว์นั้นมีความสัมพันธ์กับการเกิดการดื้อยาปฏิชีวนะของแบคทีเรีย โดยร่างกฎหมายของรัรัฐบาลกลางจำนวน 2 ฉบับ (S.742 และ H.R. 2562) ซึ่งมีใจความสำคัญที่เกี่ยวเนื่องกับการยกเลิกการใช้ยาปฏิชีวนะที่ไม่ได้มีจุดประสงค์เพื่อการรักษาในการอุตสาหกรรมการผลิตสัตว์เพื่อการบริโภคในสหรัฐอเมริกาได้ถูกเสนอเข้าในการประชุมของรัฐบาลกลาง แต่ร่างกฎหมายนี้ไม่ผ่านการเห็นชอบในที่ประชุมและมีจำเป็นต้องตกไป โดยร่างกฎหมายทั้ง 2 ฉบับดังกล่าวนั้นได้รับการรับรองและความเห็นชอบจากองค์กรทางการแพทย์และการสาธารณสุขหลายองค์กี ได้แก่ สมาคมพยาบาลแบบองค์รวมอเมริกัน (American Holistic Nurses' Association; AHNA) สมาคมการแพทย์อเมริกัน (American Medical Association; AMA) และสมาคมสาธารณสุขอเมริกา (American Public Health Association; APHA)
อย่างไรก็ตาม ถึงแม้จะมีคำมั่นสัญญาที่จะลดหรือยกเลิกการใช้เนื้อสัตว์ที่มีแหล่งที่มาจากฟาร์มที่มีการใช้ยาปฏิชีวนะจากบริษัทผลิตอาหารและภัตตาคารต่าง ๆ หลายแห่งก็ตาม การจำหน่ายยาปฏิชีวนะเพื่อใช้ในอุตสาหกรรมการผลิตสัตว์เพื่อการบริโภคนั้นก็ยังคงมีจำนวนที่เพิ่มมากขึ้นในทุก ๆ ปี ซึ่งชี้ให้เห็นว่ายังมีการใช้ยาปฏิชีวนะในการปศุสัตว์อยู่เป็นจำนวนมาก โดยในสหรัฐอเมริกา การดื้อยาปฏิชีวนะของแบคทีเรียที่มีสาเหตุมาจากการใช้ยาปฏิชีวนะในการปศุสัตว์นั้นได้เป็นประเด็นที่ได้รับการตั้งข้อสงสัยเป็นอย่างมากจากองค์การอาหารและยามาตั้งแต่ปี ค.ศ. 1977 โดยในเดือนมีนาคม ค.ศ. 2012 สภาป้องกันทรัพยากรธรรมชาติ (Natural Resources Defense Council; NRDC) และกลุ่มรณรงค์ด้านผู้บริโภคและสิ่งแวดล้อมอีก 5 กลุ่มได้ร่วมกันยื่นคำร้องต่อศาลชั้นต้นสหรัฐอเมริกาแห่งเซาท์เทิร์นดิสทริคของรัฐนิวยอร์กให้มีคำสั่งให้องค์การอาหารและยาเพิกถอนการรับรองให้ใช้ยาปฏิชีวนะในการปศุสัตว์ ซึ่งการรับรองให้ใช้ยาปฏิชีวนะในกรณีดังกล่าวนั้นถือว่าองค์การอาหารและยาละเมิดกฏข้อบังคับขององค์กรที่ตั้งไว้ตั้งแต่ ค.ศ. 1977
การศึกษาวิจัย
ยารักษาทางเลือก
การเพิ่มขึ้นอุบัติการณ์การดื้อต่อการรักษาด้วยยาปฏิชีวนะดั้งเดิมของแบคทีเรียก่อโรคหลายสายพันธุ์ที่พบในปัจจุบัน ประกอบกับการลดลงของการค้นพบยาปฏิชีวนะชนิดใหม่ รวมถึงยาที่อยู่ระหว่างการวิจัย (drug pipeline) ที่จะถูกนำมาใช้จัดการกับปัญหาดังกล่าว เป็นสัญญาณที่บ่งบอกว่าจำเป็นต้องมีการปรับเปลี่ยนกลยุทธิ์ในการคิดค้นและพัฒนายาปฏิชีวนะทางเลือกอื่นที่แตกต่างจากแบบเดิมที่เป็นอยู่ในปัจจุบัน โดยวิธีการรักษาโรคติดเชื้อจุลชีพแบบอื่นที่ไม่ใช้โครงสร้างหลักเป็นสารต้นแบบ (Non-compound approaches) ที่มีเป้าหมายการออกฤทธิ์ต่อจุลชีพ หรือเหนี่ยวนำให้แบคทีเรียก่อโรคนั้นเกิดการติดเชื้อจุลชีพอื่น อาทิ การใช้ฟาจในการรักษา และการให้วัคซีน นั้นกำลังอยู่ระหว่างการค้นคว้าพัฒนาเพื่อให้ได้ผลิตภัณฑ์ที่มีประสิทธิภาพมากที่ที่จะจัดการกับปัญหาการดื้อยาของแบคทีเรียดังข้างต้น
สารลดการดื้อยา
การเพิ่มขึ้นของอุบัติการณ์และความรุนแรงของการดื้อต่อยาปฏิชีวนะของแบคทีเรีย ทำให้นักวิจัยต่างพากันค้นคว้าทดลองเพื่อหาแนวทางในการรับมือกับปัญหาดังกล่าว กลยุทธิ์อีกอย่างหนึ่งที่ถูกนำมาใช้เพื่อแก้ปัญหานี้คือ การใช้สารลดการดื้อยา (resistance modifying agent) ร่วมกับยาปฏิชีวนะปกติในการรักษา ซึ่งสารลดการดื้อยาที่ใช้ร่วมนี้จะมีความสามารถในการลดการดื้อยาของแบคทีเรียลงได้บางส่วนหรืออาจทั้งหมด โดยสารดังกล่าวจะส่งผลยับยั้งกลไกต่างๆที่ทำเกิดการดื้อยาของแบคทีเรีย อาทิ การขับยาออก (drug efflux) จากเซลล์ รวมไปถึงส่งผลให้เซลล์แบคทีเรียมีความไวต่อยาปฏิชีวนะที่ใช้ร่วมมากขึ้น เป้าหมายการออกฤทธิ์ของสารลดการดื้อยาที่สำคัญ ได้แก่:
- การยับยั้งการขับยาออกที่ตำแหน่ง Phe-Arg-β-naphthylamide
- การยับยั้งการทำงานของเอนไซม์บีตา-แลคตาเมส เช่น กรดคลาวูลานิก และซัลแบคแตม
นอกจากนี้สารที่มีฤทธิ์กระตุ้นเมแทบอลิซึม (metabolic stimuli) อย่างน้ำตาล ก็สามารถช่วยในการกำจัดแบคทีเรียที่ทนต่อยาปฏิชีวนะบางชนิดได้โดยกระตุ้นในระบบเมแทบอลิซึมของเซลล์แบคทีเรียนั้น ๆ ตื่นตัวอยู่ตลอดเวลาการ
วัคซีน
วัคซีน เป็นสารที่ถูกนำมาใช้ในการป้องกันโรคติดเชื้อหลายชนิด โดยจะไกชักนำให้ร่างกายสร้างภูมิคุ้มกันที่จำเพาะต่อจุลินทรีย์ชนิดนั้น ๆ กล่าวคือมีฤทธิ์ชักนำการสร้างภูมิคุ้มกันอันจำเพาะกับโรค หรือเสริมภูมิคุ้มกันที่มีอยู่แล้วบางส่วนให้มีประสิทธิภาพมากขึ้น ผ่านการกระตุ้นการทำงานของแมกโครฟาจ การสร้างสารภูมิต้านทาน การอักเสบ และปฏิกิริยาการตอบสนองทั่วไปของภูมิคุ้มกันในแบบอื่น ๆ อีกหลายรูปแบบ การป้องกันโรคติดเชื้อโดยใช้วัคซีนนั้นถือเป็นอีกปัจจัยหนึ่งที่มีความสำคัญยิ่งต่อการลดลงของโรคติดเชื้อจุลชีพในทุกภูมิภาคของโลก โดยวัคซีนนั้นถือเป็นชีววัตถุที่ขึ้นจากเชื้อจุลินทรีย์หรือส่วนของเชื้อจุลินทรีย์ จะประกอบด้วยส่วนประกอบของจุลินทรีย์ที่เป็นสาเหตุของโรค (แอนติเจน) ซึ่งถูกทำให้อ่อนฤทธิ์ลง, ตาย หรือการใช้ส่วนที่เป็นพิษที่อ่อนฤทธิ์ลง (toxoid)
เฟจเพื่อการรักษาโรค
เฟจเพื่อการรักษาโรค เป็นการรักษาอีกวิธีหนึ่งที่ถูกนำมาใช้ในการรักษาโรคที่เกิดจากการติดเชื้อแบคทีเรียที่ดื้อต่อยาปฏิชีวนะ โดยการรักษาแบบเฟจเพื่อการรักษาโรคนี้จะเป็นการทำให้แบคทีเรียก่อโรคนั้น ๆ เกิดการติดเชื้อไวรัสที่มีแบคทีเรียดังกล่าวเป็นโฮสต์จำเพาะ โดยไวรัสดังกล่าวจัดเป็นแบคเทอริโอฟาจ (bacteriophage) หรือเรียกโดยย่อว่า ฟาจ เป็นไวรัสที่ต้องอาศัยอยู่กับเซลล์ของแบคทีเรียเพื่อการเจริญและเพิ่มจำนวน โดยฟาจแต่ละชนิดจะมีความจำเพาะต่อแบคทีเรียสายพันธุ์ใดสายพันธุ์หนึ่งเป็นอย่างมาก ดังนั้นฟาจดังกล่าวจึงไม่ส่งผลกระทบต่อจุลชีพอื่น ๆ หรือจุลชีพประจำถิ่นในทางเดินอาหารของโฮสต์ ซึ่งเป็นคุณสมบัติที่พบไม่ได้ในยาปฏิชีวนะที่มีใช้อยู่ในปัจจุบันแบคเทอริโอฟาจสามารถทำให้แบคทีเรียก่อโรคเกิดการติดเชื้อได้และส่งผลกระทบต่อการเจริญเติบโตหรือฆ่าเซลล์แบคทีเรียนั้น ๆ ได้โดยการทำให้เกิดการแตกออกของเซลล์ (lytic cycle) โดยฟาจจะเข้าจับกับเซลล์แบคทีเรียและแทรกสอดดีเอ็นเอของตนเข้าไปในเซลล์นั้น ซึ่งดีเอ็นเอเหล่านั้นจะถูกถอดรหัสพันธุกรรมและสังเคราะห์ส่วนประกอบชีวภาพของฟาจใหม่ขึ้นภายในเซลล์ของแบคทีเรีย ทำให้มีฟาจใหม่เกิดขึ้นภายในเซลล์แบคทีเรียจำนวนมาก จนเกิดการแตกออกของเซลล์นั้น ๆ ในที่สุด โดยฟาจใหม่ที่เกิดขึ้นนี้จะเข้าทำลายเซลล์อื่นของแบคทีเรียในสายพันธ์เดิมด้วยกระบวนการข้างต้นต่อไป การที่ฟาจมีความจำเพาะต่อแบคทีเรียสายพันธุ์หนึ่ง ๆ เป็นอย่างมากนี้จะช่วยให้แบคทีเรียอื่นที่เป็นประโยชน์ต่อโฮสต์ไม่ถูกทำลายไปด้วย อย่างไรก็ตาม การใช้ฟาจในการรักษานี้ก็มีข้อเสียเช่นเดียวกันกับการรักษาด้วยวิธีอื่น ๆ โดยจีโนมที่ฟาจแทรกสอดเข้ามาในเซลล์ของแบคทีเรียนั้นอาจมียีนหรือสารอื่นที่ก่อให้เกิดพิษสอดแทรกอยู่ ดังนั้น จึงต้องมีการศึกษาและจำแยกยีน สารประกอบหรือสารพิษต่าง ๆ จากฟาจนั้นอย่างละเอียดและรอบคอบก่อนนำมาใช้ในทางคลินิก นอกจากนี้ การศึกษาเกี่ยวกับการรักษาโรคติดเชื้อแบคทีเรียด้วยฟาจนั้นพบว่าการบริหารยาทางช่องปากและการฉีดเข้าหลอดเลือดดำนั้นมีความเสี่ยงด้านความปลอดภัยที่สูงกว่าการบริหารยาโดยการทาบนพื้นผิว (topical application) และมีความกังวลเกียวกับการตอบสนองต่อระบบภูมิคุ้มกันที่ไม่แน่นอนต่อฟาจที่จัดเป็นแอนติเจนต่อร่างกายนี้ รวมไปถึงอุปสรรคด้านกฎหมายและจริยธรรมมากมายที่จำเป็นต้องได้รับการแก้ไขเพื่อให้รองรับและสอดคล้องกับการใช้เฟจเพื่อรักษาโรค ถึงกระนั้น การใช้แบคเทอริโอฟาจเพื่อทดแทนยาต้านจุลชีพในการรักษาโรคติดเชื้อที่เกิดจากเชื้อดื้อยาหลายชนิดที่ไม่ตอบสนองต่อยาปฏิชีวนะแบบเดิม ๆ ก็ยังคงเป็นตัวเลือกที่น่าสนใจแม้ว่าจะมีความท้าทายมากมายก็ตาม
สารพฤกษเคมี
ในการคิดค้นและพัฒนายาต้านจุลชีพชนิดใหม่นั้น พืชถือว่าเป็นแหล่งที่มาสำคัญของสารประกอบที่มีฤทธิ์ต้านแบคทีเรียซึ่งอาจนำมาพัฒนาต่อยอดได้ ดังจะเห็นได้จากการใช้พืชสมุนไพรพื้นบ้านเพื่อการป้องกันและรักษาโรคที่เกิดจากการติดเชื้อจุลชีพต่าง ๆ ตั้งแต่ในอดีตจนถึงในปัจจุบัน โดยในปัจจุบัน การพัฒนายาต้านจุลชีพใหม่หลายชนิดนั้นมีแนวโน้มที่จะมุ่งความสนใจไปยังการค้นคว้าสารประกอบจากผลิตภัณฑ์ธรรมชาติที่มีคุณสมบัติในการต้านจุลชีพ โดยเรียกสารเหล่านั้นว่าเป็นสารในกลุ่ม 'antibiotic-ome' (ซึ่งมีการให้นิยามว่าหมายถึง ผลิตภัณฑ์จากธรรมชาติที่มีฤทธิ์ต้านแบคทีเรีย) ซึ่งมีประโยชน์เป็นอย่างมากสำหรับการค้นคว้ายาต้านเชื้อแบคทีเรียในยุคปัจจุบันที่มีการศึกษาลึกถึงระดับจีโนม โดยสารในพืชสมุนไพรที่ค้นพบว่ามีฤทธิ์ทางยานั้นจะถูกเรียกว่า สารพฤกษเคมี ซึ่งสารพฤกษเคมีบางชนิด ได้แก่ แทนนิน แอลคาลอยด์ เทอร์พีนอยด์ และฟลาโวนอยด์ พบว่ามีสมบัติในการต้านแบคทีเรียด้วย นอกจากนี้ ผลการทดลองในเนื้อเยื่อนอกร่างกายมุนษย์ (in vitro) ของผลิตภัณฑ์เสริมอาหารจากธรรมชาติที่มีฤทธิ์ต้านอนุมูลอิสระบางชนิดที่มีส่วนประกอบเป็นสารพฤกษเคมี (สารกลุ่มโพลีฟีนอล) เช่น สารสกัดจากเมล็ดองุ่น พบว่าก็มีคุณสมบัติในการต้านแบคทีเรียเช่นกัน โดยสารพฤกษเคมีที่มีฤทธิ์ต้านแบคทีเรียเหล่านี้มีกลไกการออกฤทธิ์ที่หลากหลายแตกต่างกันออกไปขึ้น โดยอาจออกฤทธิ์ยับยั้งการสังเคราะห์เปบทิโดไกลแคนซึ่งเป็นส่วนประกอบของผนังเซลล์แบคทีเรีย ทำให้เกิดความเสียหายต่อเยื่อหุ้มเซลล์ของแบคทีเรีย ปรับเปลี่ยนสมบัติความไม่เข้ากันกับน้ำ (hydrophobicity) ของพื้นผิวเยื่อหุ้มเซลล์แบคทีเรีย หรืออาจกระตุ้นระบบควอรัมเซนซิง (quorum-sensing) ของแบคทีเรียให้ผลิตสารที่เป็นสัญญาณระบุตำแหน่งที่เอื้อต่อการออกฤทธิ์ของยาปฏิชีวนะ อย่างไรก็ตาม ถึงแม้ว่าในปัจจุบันอุบัติการณ์และความรุนแรงของการเกิดแบคทีเรียดื้อยาจะเพิ่มสูงขึ้นเป็นอย่างมาก แต่ยาปฏิชีวนะชนิดใหม่ที่เป็นอนุพันธ์ของสารประกอบจากสมุนไพรซึ่งได้รับการคาดหวังว่าจะช่วยบรรเทาความรุนแรงของภาวะฉุกเฉินดังกล่าวลงนั้น ยังอยู่ในระหว่างการศึกษาค้นคว้าในห้องปฏิบัติการเท่านั้น
การพัฒนายาปฏิชีวนะชนิดใหม่
ในเดือนเมษายน ค.ศ. 2013 สมาคมโรคติดเชื้อแห่งสหรัฐอเมริกา (Infectious Disease Society of America; IDSA) reported that the weak antibiotic pipeline นั้นไม่มีความสัมพันธ์กับความสามารถในการดื้อยาปฏิชีวนะของแบคทีเรียที่เพิ่มมากขึ้น โดยนับตั้งแต่ ค.ศ. 2009 เป็นต้นมา พบว่ามีการค้นพบยาปฏิชีวนะชนิดใหม่และได้รับการรับรองให้ใช้กับมนุษย์ในสหรัฐอเมริกาเพียง 2 ชนิดเท่านั้น โดยในช่วงระยะเวลาหลายทศวรรษที่ผ่านมานั้น ยาปฏิชีวนะชนิดใหม่สำหรับมนุษย์ที่ได้รับการรับรองให้ผลิตเชิงการค้านั้นมีจำนวนที่ลดลงอย่างต่อเนื่องในทุกๆปี โดยในรายงานดังกล่าวระบุว่ามียาปฏิชีวนะชนิดใหม่จำนวน 7 รายการที่ออกฤทธิ์ต้านเชื้อแบคทีเรียแกรมลบสกุลบาซิลลัส (Gram-negative bacilli; GNB) ที่กำลังอยู่ระหว่างการศึกษาวิจัยทางคลินิกในขั้นที่ 2 และขั้นที่ 3 ถึงกระนั้น ยาดังกล่าวก็ไม่ได้มีขอบเขตการออกฤทธิ์ครอบคลุมเชื้อแบคทีเรียแกรมลบสกุลบาซิลลัสที่พบการดื้อยาปฏิชีวนะในปัจจุบัน ตัวอย่างยาปฏิชีวนะชนิดใหม่ที่ถูกค้นพบหรือการนำยาปฏิชีวนะชนิดเดิมมาใช้ร่วมกับยาอื่นเพื่อป้องกันการเกิดการดื้อยาของแบคทีเรียหรือขยายขอบเขตการออกฤทธิ์ของยาปฏิชีวนะชนิดนั้นให้ครอบคลุมเชื้อแบคทีเรียได้หลากหลายมากขึ้น เช่น:
- เซฟโตโลเซน/ทาโซแบคแตม (CXA-201; CXA-101/ทาโซแบคแตม) : เป็นยาสูตรผสมระหว่างเซฟาโลสปอรินที่มีฤทธิ์ต้านแบคทีเรียสกุลซูโดโมแนสกับยาที่ยับยั้งเอนไซม์บีตา-แลคตาเมส (ยับยั้งการสังเคราะห์ผนังเซลล์) ได้รับการรับรองจากองค์การอาหารและยาของสหรัฐอเมริกาเมื่อวันที่ 19 ธันวาคม ค.ศ. 2014
- เซฟตาซิดิม/อะวิแบคแตม (เซฟตาซิดิม/NXL104) : เป็นยาสูตรผสมระหว่างเซฟาโลสปอรินที่มีฤทธิ์ต้านแบคทีเรียสกุลซูโดโมแนสกับยาที่ยับยั้งเอนไซม์บีตา-แลคตาเมส (ยับยั้งการสังเคราะห์ผนังเซลล์) ขณะนี้กำลังอยู่ในขั้นตอนการศึกษาทางคลินิกระยะที่ 3
- เซฟตารอลีน/อะวิแบคแตม (CPT-อะวิแบคแตม; เซฟตารอลีน/NXL104) : เป็นยาสูตรผสมระหว่างเซฟาโลสปอรินที่มีฤทธิ์ต้านสแตปฟิโลคอคคัส ออเรียสที่ดื้อต่อยาเมทิซิลลิน (Methicillin-resistant Staphylococcus aureus; MRSA) กับยาที่ยับยั้งเอนไซม์บีตา-แลคตาเมส (ยับยั้งการสังเคราะห์ผนังเซลล์)
- อีมิพีแนม/MK-7655: เป็นยาสูตรผสมระหว่างยาปฏิชีวนะในกลุ่มคาร์บาพีแนมกับยาที่ยับยั้งเอนไซม์บีตา-แลคตาเมส (ยับยั้งการสังเคราะห์ผนังเซลล์) ปัจจุบันกำลังอยู่ระหว่างการศึกษาวิจัยทางคลินิกในระยะที่ 2
- พลาโซมัยซิน (ACHN-490) : เป็นยาปฏิชีวนะในกลุ่มอะมิโนไกลโคไซด์ (ยับยั้งการสังเคราะห์โปรตีน) โดยข้อมูล ณ เดือนตุลาคม ค.ศ. 2017 คำร้องขอขึ้นทะเบียนยาใหม่ของพลาโซมัยซินกำลังอยู่ระหว่างการพิจารณาอนุมัติขององค์การอาหารและยาของสหรัฐอเมริกา
- อีวาราไซคลีน (TP-434) : อนุพันธ์ของเตเตราไซคลีนที่ได้จากการสังเคราะห์ ซึ่งจะออกฤทธิ์ยับยั้งการทำงานของไรโบโซมของแบคทีเรีย ทำให้การสังเคราะห์โปรตีนในเซลล์เกิดความผิดพลาดหรือหยุดชะงักลง โดยยานี้ถูกพัฒนาขึ้นโดยบริษัท Tetraphase องค์การอาหารและยาของสหรัฐอเมริกาให้การรับรองเมื่อวันที่ 27 สิงหาคม ค.ศ. 2018
- ไบรลาซิดิน (PMX-30063): เป็นยาปฏิชีวนะชนิดใหม่ที่ออกฤทธิ์แตกต่างจากยาปฏิชีวนะอื่นที่มีอยู่ในปัจจุบัน โดยจัดเป็นเปปไทด์ต้านจุลชีพ (antimicrobial peptides) หรือ เปปไทด์ระบบภูมิต้านทาน (host defense peptide) โดยยานี้จะให้เกิดการแตกออกของเยื่อหุ้มเซลล์ของแบคทีเรีย ปัจจุบันกำลังอยู่ระหว่างการศึกษาวิจัยทางคลินิกในระยะที่ 2
การศึกษาวิจัยเกี่ยวกับสารที่ได้จากแบคทีเรียสกุลสเตรปโตมัยซิสนั้นได้รับการคาดหวังจากวงการสาธารณสุขเป็นอย่างยิ่งว่าจะช่วยให้ค้นพบยาปฏิชีวนะชนิดใหม่ได้หลากหลายยิ่งขึ้น โดยเฉพาะอย่างยิ่งยาปฏิชีวนะที่ออกฤทธิ์ต้านสแตปฟิโลคอคคัส ออเรียสที่ดื้อต่อยาเมทิซิลลิน (Methicillin-resistant Staphylococcus aureus; MRSA) และแบคทีเรียอื่นที่ดื้อต่อยาปฏิชีวนะที่มีใช้อยู่ทั่วไปในปัจจุบัน ความพยายามที่จะทำการศึกษาในประเด็นดังกล่าวของจอห์น อินนส์ เซ็นเตอร์และมหาวิทยาลัยหลายแห่งในสหราชอาณาจักร ซึ่งได้รับการสนับสนุนจากสภาวิจัยด้านเทคโนโลยีชีวภาพและวิทยาศาสตร์ชีวภาพ (The Biotechnology and Biological Sciences Research Council; BBSRC) ทำให้มีการก่อตั้งบริษัทต่าง ๆ เพื่อดำเนินงานด้านการวิจัยและพัฒนายาปฏิชีวนะชนิดใหม่เกิดขึ้นเป็นจำนวนมาก ตัวอย่างเช่น บริษัทโนวาคตาไบโอซิสเตมส์ (Novacta Biosystems Ltd.) ซึ่งเป็นบริษัทที่พัฒนาและออกแบบสารประกอบ NVB302 ซึ่งจัดเป็นยาปฏิชีวนะในกลุ่มแลนติไบโอติก ชนิดบี (type-b lantibiotic) เพื่อรักษาการติดเชื้อแบคทีเรีย Clostridium difficile โดยปัจจุบันยานี้กำลังอยู่ระหว่างการศึกษาวิจัยทางคลินิกในระยะที่ 1 อย่างไรก็ตาม ความเป็นไปได้ในการคิดค้นและพัฒนายาใหม่นั้นขึ้นอยู่กับการกำหนดข้อบังคับที่เกี่ยวเนื่องการทดลองทางคลินิกขององค์การอาหารและยา รวมไปถึงแรงจูงใจทางเศรษฐกิจที่เหมาะสมอาจชักชวนให้บริษัทยากล้าที่จะลงทุนในความพยายามนี้ ใน ค.ศ. 2013 เพื่อตอบสนองต่อการดื้อยาปฏิชีวนะของแบคทีเรียที่มีจำนวนและความรุนแรงที่เพิ่มมากขึ้น รัฐสภาสหรัฐได้มีมติเห็นชอบผ่านร่างกฎหมายการพัฒนายาปฏิชีวนะเพื่อการรักษาผู้ป่วยขึ้นสูง (Antibiotic Development to Advance Patient Treatment; ADAPT) โดยภายใต้การดำเนินงานนี้ องค์การอาหารและยาจะสามารถให้การรับรองยาปฏิชีวนะและยาต้านเชื้อราใด ๆ ที่ทำการศึกษาในกลุ่มตัวอย่างที่เล็กลงกว่าปกติสำหรับการรักษาโรคติดเชื้อที่มีความรุนแรงจนอาจก่อให้เกิดอันตรายแก่ชีวิตของผู้ป่วย ส่วนศูนย์ควบคุมและป้องกันโรค (Centers for Disease Control and Prevention; CDC) จะทำหน้าที่เฝ้าระวังและติดตามการใช้ยาปฏิชีวนะในด้านต่าง ๆ รวมไปถึงการเกิดการดื้อยาปฏิชีวนะของแบคทีเรีย และตีพิมพ์เผยแพร่ข้อมูลหรือสถานการณ์นั้นให้แก่หน่วยงานอื่นที่เกียวเนื่อง นอกจากนี้ องค์การอาหารและยายังมีหน้าที่ในการกำหนดเกณฑ์ต่าง ๆ ที่ใช้ทดสอบความไวของแบคทีเรียต่อยาปฏิชีวนะใด ๆ ด้วย อาทิ "เกณฑ์การตีความการทดสอบความไวของจุลินทรีย์" หรือ "ค่าจุดตัดความไวของยา" (breakpoint) และให้ข้อมูลที่ถูกต้องเหล่านี้แก่บุคลากรทางการแพทย์ ซึ่งการเกิดขึ้นของการดำเนินงานนี้เป็นผลมาจากคำแนะนำของอัลลาน คูเกลล์ (Allan Coukell) ผู้อำนวยการอาวุโสขององค์กรการกุศลพิว (The Pew Charitable Trusts) ที่ได้แสดงความคิดเห็นในประเด็นที่เกี่ยวกับการพัฒนายาปฏิชีวนะชนิดใหม่เพื่อตอบสนองความฉุกเฉินของแบคทีเรียดื้อยาว่า "เพื่อที่จะให้การศึกษาวิจัยทางคลินิกนั้นสามารถทำได้ง่ายมากขึ้น ควรยินยอมให้นักพัฒนายาใช้ข้อมูลและตัวอย่างในการศึกษาทางคลินิกที่น้อยลง และองค์การอาหารและยาก็ต้องแสดงให้เห็นได้แน่ชัดว่าสามารถยอมรับความเสี่ยงที่เพิ่มมากขึ้นเมื่อคิดคำนวณโทษ–ประสิทธิผลที่อาจได้จากยาเหล่านั้น"
ดูเพิ่ม
อ่านเพิ่ม
- Davies, Julian; Davies, Dorothy (1 กันยายน 2010). "Origins and Evolution of Antibiotic Resistance". Microbiology and Molecular Biology Reviews : MMBR. 74 (3): 417–433. doi:10.1128/MMBR.00016-10. ISSN 1092-2172. PMC 2937522. PMID 20805405.
- "Antibiotics: MedlinePlus". NIH.gov. สืบค้นเมื่อ 19 กรกฎาคม 2016.
- "WHO's first global report on antibiotic resistance reveals serious, worldwide threat to public health". WHO.
- Pugh Richard (2015). "Short-course versus long-course antibiotic treatment for hospital-acquired pneumonia in adult intensive care patients | Cochrane". Reviews. doi:10.1002/14651858.CD007577.pub3.
- Giedraitienė, Agnė; Vitkauskienė, Astra; Naginienė, Rima; Pavilonis, Alvydas (1 มกราคม 2011). "Antibiotic resistance mechanisms of clinically important bacteria". Medicina (Kaunas, Lithuania). 47 (3): 137–146. ISSN 1648-9144. PMID 21822035.
- Robert Berkow, บ.ก. (September 1999). The Merck Manual of Medical Information (Home ed.). ISBN 0-671-02727-1.
แหล่งข้อมูลอื่น
|
คอมมอนส์ มีภาพและสื่อเกี่ยวกับ: ยาปฏิชีวนะ |
- Antibiotic News from Genome News Network (GNN)
- Bruce Sterling's Bitter Resistance
- JAAPA: New antibiotics useful in primary care
- "A new method for controlling bacterial activity without antibiotics", Research conducted at the Hebrew University, คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 8 กุมภาพันธ์ 2006
|
ยาต้านจุลชีพ − ประเด็นด้านสังคมและวัฒนธรรม
| |
|---|---|
| ประเภทของยาต้านจุลชีพ | |
| ประเด็นด้านสังคม | |
| เภสัชวิทยา | |
|
ทางเดินอาหาร/ เมแทบอลิซึม (A) |
กรดกระเพาะ (ยาลดกรด, สารต้านตัวรับ H2 , ยายับยั้งการหลั่งกรด) • ยาแก้อาเจียน • ยาระบาย • ยาแก้ท้องร่วง • ยาลดความอ้วน • ยาต้านเบาหวาน • วิตามิน • เกลือแร่
|
|---|---|
|
เลือดและอวัยวะ สร้างเลือด (B) |
|
|
ระบบหัวใจ และหลอดเลือด (C) |
ยารักษาโรคหัวใจ/ยาแก้อาการปวดเค้นหัวใจ (คาร์ดิแอคไกลโคไซด์ , ยาต้านภาวะหัวใจเสียจังหวะ , ยากระตุ้นหัวใจ) • ยาลดความดัน • ยาขับปัสสาวะ • สารขยายหลอดเลือด • เบต้า บล็อกเกอร์ • แคลเซียมแชนแนลบล็อกเกอร์ • ระบบเรนิน-แองจิโอเทนซิน (เอซีอีอินฮิบิเตอร์ , แองกิโอเทนซินรีเซพเตอร์บล๊อคเกอร์ , เรนินอินฮิบิเตอร์) • ยาลดไขมันในเส้นเลือด (สแตติน , ไฟเบรต , ไบล์แอซิดซีเควสแตรนต์) |
| ผิวหนัง (D) | |
| ระบบสืบพันธุ์ (G) | |
| ระบบต่อมไร้ท่อ (H) | |
|
การติดเชื้อและ การติดเชื้อปรสิต (J, P, QI) |
|
| มะเร็ง (L01-L02) | |
| โรคทางระบบ ภูมิคุ้มกัน (L03-L04) |
|
| กล้ามเนื้อ กระดูก และข้อต่อ (M) | |
| สมองและระบบประสาท (N) | |
| ระบบทางเดินหายใจ (R) | |
| อวัยวะรับความรู้สึก (S) | |
| อื่น ๆ (V) | |